
| A、未用标准液润洗碱式滴定管 |
| B、滴定终点读数时,俯视滴定管的刻度,其它操作均正确 |
| C、盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| D、滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:
| A、钠是银白色金属,硬度很大 |
| B、将金属钠放在石棉网上用酒精灯加热后,金属钠剧烈燃烧,产生黄色火焰,生成Na2O2 |
| C、金属钠在空气中燃烧,生成氧化钠 |
| D、金属钠的熔点很高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
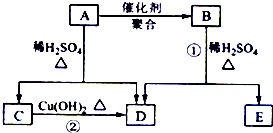 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如图所示:已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO.根据以上信息回答下列问题:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如图所示:已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO.根据以上信息回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
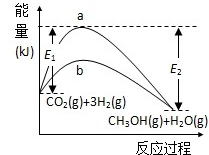 一定条件下发生反应:
一定条件下发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:
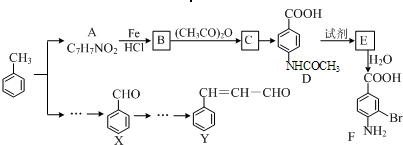

| NaOH |
| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氖气含Ne原子数为2NA |
| B、标准状况下,22.4L氨气中所含的氢原子总数为3NA |
| C、1L 1mol?L-1的盐酸中含HCl的分子数为NA |
| D、1mol由O2和CO2组成的混合气体中,含氧原子的总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有① | B、①② |
| C、②③ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com