
分析 (1)根据所给的条件反应,结合要求的目标反应,将条件反应调整计量数并做相应的加减得目标反应,反应热做相应的变化即可;
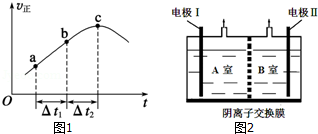
(2)①反应达平衡的根本标志是V正=V逆,而c点的只是V正最大而已;
②容器恒容绝热,SO2(g)+NO2(g)?NO(g)+SO3 (g)△H<0,反应放热,若在该容器中加入:Ⅰ:1molSO2(g)和1molNO2(g),则开始反应放热;若在容器中加入II:1molSO3(g)和1mol NO(g),则开始时反应吸热,据此分析平衡常数;
(3)通过A室产生了N2,可知A极的电解质溶液为NaNO3和NaNO2的混合溶液,NO2-在A极放电为N2,则A为阴极;则B极为阳极,电解质溶液为NaOH溶液,OH-在B极放电,据此分析;
(4)设出NO的体积为XL,NO2的体积为YL,则有X+Y=6 ①然后根据和氨气反应时得失电子数守恒可有:2X+4Y=7×3 ②将两式联立解答.
解答 解:(1)已知:2SO2(g)+O2 (g)?2SO3 (g)△H=-196.6kJ•mol-1 ①
2NO(g)+O2 (g)?2NO2 (g)△H=-113.0kJ•mol-1 ②
根据盖斯定律,将$\frac{1}{2}$(①-②)可得:SO2(g)+NO2(g)?NO(g)+SO3 (g)△H=$\frac{1}{2}$[(-196.6kJ•mol-1)-(-113.0kJ•mol-1)]=-41.6KJ/mol,该反应的焓变△H<0,为放热反应,
故答案为:放热;
(2)①化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,c点对应的正反应速率显然还在改变,故一定未达平衡,
故答案为:未达;
②容器恒容绝热,SO2(g)+NO2(g)?NO(g)+SO3 (g)△H<0,反应放热,若在该容器中加入:Ⅰ:1molSO2(g)和1molNO2(g),则开始反应放热,温度升高平衡左移,K减小;若在容器中加入II:1molSO3(g)和1mol NO(g),则开始时反应吸热,温度降低平衡右移,K增大,故该反应的平衡常数Ⅰ<Ⅱ,
故答案为:<;
(3)通过A室产生了N2,可知I极的电解质溶液为NaNO3和NaNO2的混合溶液,NO2-在I放电为N2,则A为阴极;则II极为阳极,电解质溶液为NaOH溶液,OH-在II极放电.
①电极I为阴极,由于B室为NaOH溶液,且II极为阳极,故在II极放电的是氢氧根:4OH--4e-=O2↑+2H2O,即产生的气体为氧气,
故答案为:阴极;O2;
②NO2-在阴极得电子被还原为氮气,结合B室的溶液是中性溶液,故放电的方程式为:2NO2-+6e-+6H2O=8OH-+N2↑,
故答案为:2NO2-+6e-+6H2O=8OH-+N2↑;
(4)设出NO的体积为XL,NO2的体积为YL,根据混合气体的体积为6L,则有X+Y=6 ①
氨气反应时,NO和NO2得电子,而氨气失电子,根据得失电子数守恒可有:2X+4Y=7×3 ②
将两式联立即可解得X=1.5,Y=4.5,则有X:Y=1:3,
故答案为:1:3.
点评 本题考查较为综合,涉及本题考查了盖斯定律的应用、化学平衡常数的大小比较以及电化学知识的运用,注意掌握盖斯定律的内容、电解原理,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 植物油存放过久,会有一种难闻的“哈喇”味,但不影响食用 | |
| B. | 葡萄糖能发生水解反应 | |
| C. | 淀粉和纤维素水解的最终产物是葡萄糖 | |
| D. | 氨基酸分子中含有氨基和羧基,因此具有两性,但蛋白质没有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
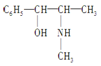 麻黄素中含氧官能团的名称是羟基,属于醇类(填“醇”或“酚”).
麻黄素中含氧官能团的名称是羟基,属于醇类(填“醇”或“酚”).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
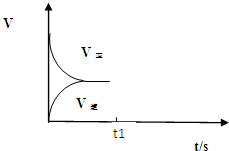 化工工业中常用乙苯脱氢的方法制备苯乙烯.
化工工业中常用乙苯脱氢的方法制备苯乙烯.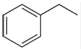 (g)→
(g)→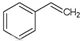 (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol; (g)+CO(g)+H2O(g) △H=+158.8 kJ/mol
(g)+CO(g)+H2O(g) △H=+158.8 kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ/mol,T1温度下不同时段产生O2的量,见表:
一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ/mol,T1温度下不同时段产生O2的量,见表:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 1.0 | 1.6 | 2.0 | 2.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
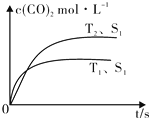 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
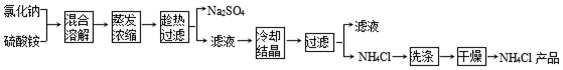
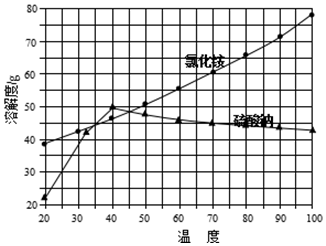
| 操作步骤 | 现象 | 结论 |
| 取少量氯化铵产品于试管底部,加热 | 如果试管底部没有固体剩余 | 表明氯化铵产品纯净 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com