
| A. | 除去CO2 中少量CO,通过灼热氧化铜 | |
| B. | 除去NO中少量NO2,气体通入足量水中后,用浓硫酸干燥 | |
| C. | 除去KCl固体中少量K2CO3,加入足量盐酸后,蒸发、结晶 | |
| D. | 除去CuSO4 溶液中Fe2(SO4)3 杂质,加入足量铜粉,过滤 |
分析 A.CO与CuO反应生成二氧化碳;
B.二氧化氮与水反应生成NO;
C.K2CO3与盐酸反应生成KCl;
D.Fe2(SO4)3 与Cu反应生成CuSO4、FeSO4.
解答 解:A.CO与CuO反应生成二氧化碳,则通过灼热氧化铜可除杂,故A正确;
B.二氧化氮与水反应生成NO,则气体通入足量水中后,用浓硫酸干燥可除杂,故B正确;
C.K2CO3与盐酸反应生成KCl,则加入足量盐酸后,蒸发、结晶可除杂,故C正确;
D.Fe2(SO4)3 与Cu反应生成CuSO4、FeSO4,引入新杂质,不能除杂,应加CuO、过滤除杂,故D错误;
故选D.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意把握物质的性质、性质差异及发生的反应,除杂时不能引入新的杂质,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 1:3 | C. | 2:3 | D. | 3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②④⑤ | C. | ③④⑤ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
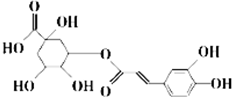 中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )| A. | 绿原酸可通过酯化反应人工合成 | |
| B. | 1 mol绿原酸能与2molBr2发生加成反应 | |
| C. | 1mol绿原酸能与6molNa发生置换反应 | |
| D. | 绿原酸能与NaHCO3溶液发生复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工厂通常采用20 Mpa~50 MPa压强,以提高原料的利用率 | |
| C. | 打开啤酒瓶盖后有大量泡沫溢出 | |
| D. | 夏天将食品储藏在冰箱中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
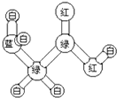 有机物A是构成营养素的基础物质,A的球棍模型如图所示,图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子.回答下列问题:
有机物A是构成营养素的基础物质,A的球棍模型如图所示,图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(A)=0.5 mol/(L•min) | B. | υ(B)=0.3 mol/(L•min) | ||
| C. | υ(C)=0.03 mol/(L•s) | D. | υ(D)=1 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com