
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源:2012--2013学年新疆乌鲁木齐市高二下学期期中考试化学试卷(特长班)(解析版) 题型:选择题
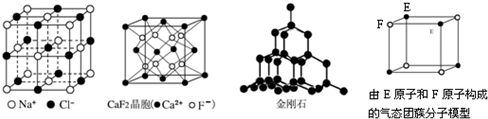
根据下列结构示意图,判断下列说法中不正确的是
A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数目比为1:2
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源:2010-2011学年四川成都外国语学校高三10月月考化学卷 题型:选择题
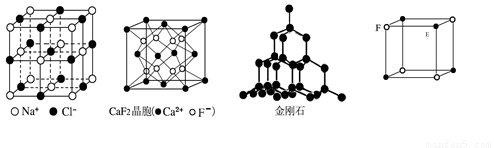
根据下列结构示意图,判断下列说法中不正确的是( )
A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数目比为1:2
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源:2010-2011学年吉林省高三上学期第二次教学质量检测化学卷 题型:选择题
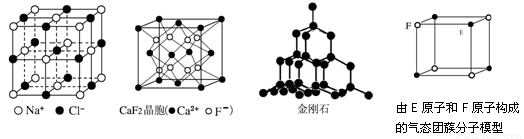
根据下列结构示意图,判断下列说法中不正确的是 ( )
A.在NaCl晶体中,距Na+最近的多个Cl-构成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数之比为1:2
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源:2010年重庆市高三秋季开学测试化学(理)试题 题型:选择题
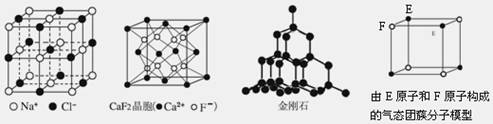
根据下列结构示意图,判断下列说法中不正确的是 ( )

A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数目比为1:2
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com