
【题目】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
I.污染物SO2、NO2经O2预处理后用CaSO3悬浊液吸收,可减少尾气中SO2、NOx的含量。
T℃时,O2氧化烟气中SO2、NOx的主要反应的热化学方程式为:
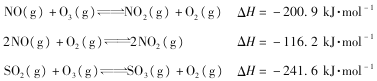
(1)T℃时,反应3NO(g)+O3(g) ![]() 3NO2(g)的△H=_______________kJ.mol-1。
3NO2(g)的△H=_______________kJ.mol-1。
(2)T℃时,将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
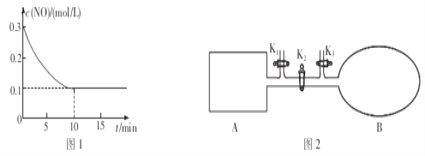
①T℃时,反应3NO(g)+O3(g)![]() 3NO2(g)的平衡常数K=______________。
3NO2(g)的平衡常数K=______________。
②不能说明反应达到平衡状态的是______________。
A.气体颜色不再改变 B.气体的平均摩尔质量不再改变
C.气体的密度不再改变 D.单位时间内生成O3和NO2物质的量之比为1:3
II.NO2的二聚体N2O4是火箭中常用氧化剂。完成下列问题:
(3)如图2所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊。关闭K2,将各1 molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL(忽略导管中的气体体积)。
①若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)=________________。
②若打开K2,平衡后B容器的体积缩至0.4aL,则打开K2之前,气球B体积为__________L。
③若平衡后在A容器中再充入0.5molN2O4,则重新到达平衡后,平衡混合气中NO2的体积分数______________(填“变大”“变小”或“不变”)。
【答案】 -317.1 240(或240 L.mol一1) C ![]() 0.7a 变小
0.7a 变小
【解析】Ⅰ.(1)①NO(g)+O3(g)NO2(g)+O2(g)△H=-200.9 kJ/mol,②2NO(g)+O2(g)2NO2(g)△H=-116.2 kJ/mol,①+②得到T℃时,反应3NO(g)+O3(g)3NO2(g)的△H=-317.1kJ/mol,故答案为:-317.1;
(2)①T℃时,将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,图象分析可知平衡状态NO浓度为0.1mol/L,10min达到平衡,
3NO(g)+O3(g)3NO2(g)
起始量(mol/L) 0.3 0.1 0
变化量(mol/L) 0.2 ![]() 0.2
0.2
平衡量(mol/L) 0.1 ![]() 0.2
0.2
K=![]() =240,故答案为:240;
=240,故答案为:240;
②反应3NO(g)+O3(g)3NO2(g)的△H=-317.1kJ/mol,反应是气体体积减小的放热反应。A.气体颜色不再改变,说明二氧化氮浓度不变,反应达到平衡状态,故A不符合;B.反应前后气体质量不变,物质的量变化,当气体的平均摩尔质量不再改变说明反应达到平衡状态,故B不符合;C.气体质量和体积不变,气体的密度始终不改变,不能说明反应达到平衡状态,故C符合;D.反应速率之比等于化学方程式计量数之比为正反应速率之比,当单位时间内生成O3和NO2物质的量之比为1:3,表明正逆反应速率相同,反应达到平衡状态,故D不符合;故答案为:C;
Ⅱ.(3)①关闭K2,将各1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL,若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,设生成四氧化二氮为x
2NO2(g)N2O4(g)
起始量 1 0
变化量 2x x
平衡量 1-2x x
1-2x+x=0.8×1,解得:x=0.2mol,则平均化学反应速率v(NO2)=![]() =
=![]() mol/(Ls),故答案为:
mol/(Ls),故答案为:![]() mol/(Ls);
mol/(Ls);
②打开K2,则相当于是在等温等压时的平衡,因此平衡是等效的,由于此时反应物的物质的量是B中的二倍,所以打开K2之前,气球B体积为(aL+0.4aL)÷2=0.7aL,故答案为:0.7a;
③若平衡后在A容器中再充入0.5molN2O4,相当于中等压强,平衡正向进行,则重新到达平衡后,平衡混合气中NO2的体积分数变小,故答案为:变小。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】下列有关糖类的说法,错误的是( )
A.糖类由碳、氢、氧三种元素组成
B.糖类是人类食物的重要成分之一
C.在人类食物所提供的总能量中大约有75%来自糖类
D.淀粉在人体内经酶的催化作用,与水发生一系列反应,最终变为蔗糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() U是重要的核工业原料,下列有关
U是重要的核工业原料,下列有关 ![]() U的说法正确的是( )
U的说法正确的是( )
A.![]() U与
U与 ![]() U互为同素异形体
U互为同素异形体
B.![]() U与
U与 ![]() U互为同位素
U互为同位素
C.![]() U原子核中含有92个中子
U原子核中含有92个中子
D.![]() U原子核外有143个电子
U原子核外有143个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中正确的是( )
A.离子还原性:S2->Cl->Br->I-
B.氧化性:F2>Cl2>Br2>S
C.酸性:H2SO4>HClO4>H3PO4
D.非金属性:F>Cl>S>O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是
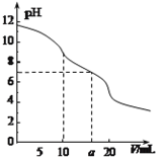
A. 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B. 当V=5时:c(CO32—)+c(HCO3-)+c(H2CO3)=c(Cl-)
C. 当V=10时:c(Na+)>c(HCO3-)>c(CO32—)>c(H2CO3)
D. 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种物质中 ①Ne ②H2O ③NH3④KOH ⑤Na2O(填写序号):只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列观点正确的是( )
A.H2O2中只存在极性键
B.在氧化钠中,只存在氧离子和钠离子的静电吸引作用
C.某化合物熔融态能导电,该化合物中一定有离子键
D.Na2O和Na2O2所含化学键类型完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com