
【题目】已知:![]() 。将一定量的硫酸酸化的KMnO4溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示。下列说法错误的是
。将一定量的硫酸酸化的KMnO4溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示。下列说法错误的是
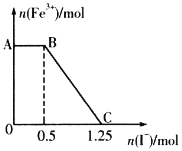
A.AB段发生I-被![]() 氧化的反应
氧化的反应
B.BC段发生的反应为![]()
C.开始时加入KMnO4的物质的量为0.15mol
D.开始时加入FeSO4的物质的量为1.25mol
科目:高中化学 来源: 题型:
【题目】观察下列几个装置示意图,有关叙述不正确的是( )
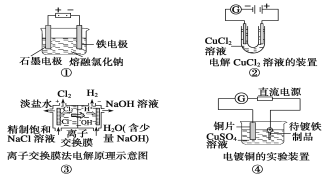
A.装置①工业上可用于生产金属钠,电解过程中石墨电极产生氯气,此法也可用于生产活泼金属镁、铝等
B.装置②中随着电解的进行右边电极会产生红色的铜,并且电流计示数不断变小
C.装置③中的离子交换膜具有很强的选择性,只允许某类离子(如Na+)通过
D.装置④的待镀铁制品应与电源负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化铁加热易升华,遇潮湿空气易变质。在实验室中,可以采用如下装置和药品制取较纯的无水氯化铁固体。
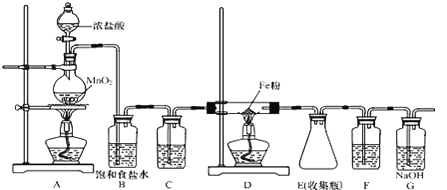
(1)制取氯化铁时,应先点燃_____(填“A”或“D”)处的酒精灯,制取氯化铁的化学方程式为_____。
(2)C、F装置中所装试剂相同,试剂均为________。
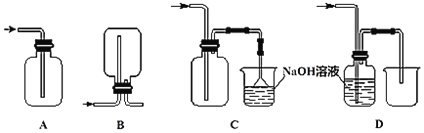
(3)下列收集Cl2的正确装置是______。
(4)G装置中反应的离子方程式为________________________________。
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为______(选填序号,下同);写出溶液变血红色的离子方程式:_____________,若溶液未变血红色,推断固体物质的成分为______。
A.只有 FeCl3 B.只有Fe C.一定有FeCl3 D.一定有Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,实验小组同学进行如图实验,下列说法错误的是
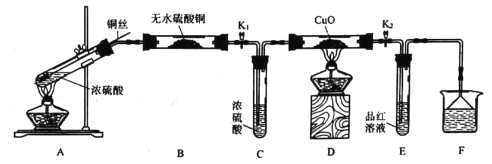
A.F中可以盛放酸性KMnO4溶液
B.为确认有硫酸铜生成,可向反应后的A中加水
C.此实验设计不能排除浓硫酸中的水是否影响B装置现象的判断
D.可通过D中固体不变色而E中溶液褪色的现象证明浓硫酸中硫元素的氧化性强于氢元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制450mL 1.0mol·L-1 NaOH溶液,下列说法正确的是
A.用托盘天平称取18.0g NaOH固体
B.在烧杯中溶解NaOH固体后立即转移至容量瓶
C.定容时,改用胶头滴管加水至凹液面最低点与刻度线相切
D.NaOH固体在烧杯中称量时间过长,所配NaOH溶液浓度偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板中铜元素含量较高,为充分利用资源,变废为宝实验小组探究利用废旧印刷电路板来制备胆矾,具体流程如图所示:
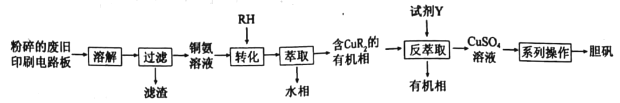
请回答:
(1)“溶解”过程中,为选择合适的溶解试剂,查阅资料后,小组同学设计如下实验。
实验编号 | 铜片质量/g | 试剂及用量 | 现象 |
1号 | 0.5 | 30%H2O250mL、蒸馏水8mL | 10h后,溶液变为浅蓝色,铜片表面附着蓝色沉淀 |
2号 | 0.5 | 30%H2O250mL、5mol·L-1H2SO48mL | 开始铜片表面有气泡生成(先慢后快,40min后,溶液蓝色明显铜片表面光亮 |
3号 | 0.5 | 30%H2O250mL、5mol·L-1氨水8mL | 立即产生大量气泡溶液为深蓝色,铜片表面附着少量蓝色沉淀 |
注:深蓝色溶液为铜氨溶液。
①1号实验中发生反应的化学方程式为______________。
②实验室检验2号实验中产生气体的操作和现象为______________。
③与2号实验相比,3号实验的优点是生成了铜氨配合物,加快了反应速率;其不足之处为______________。
④为弥补3号实验的不足,该小组继续进行改进,设计了4号实验(见下表,并得到了预期的实验现象。
实验编号 | 铜片质量/g | 试剂及用量 | 现象 |
4号 | 0.5 | 30%H2O250mL5mol·L-1氨水8mL和适量试剂X | 立即产生大量气泡,溶液为深蓝色,铜片表面仍光亮 |
则4号实验中,试剂x应为______________。
(2)“转化”时铜氨溶液中的Cu(NH3)42+与有机物RH发生反应的离子方程式为______________。“反萃取”过程中,所加试剂Y的化学式为______________。
(3)“系列操作”具体指_____________(填选项字母)。
A.蒸发浓缩、趁热过滤、洗涤、干燥
B.蒸发浓缩至溶液表面出现晶膜后停止加热,冷却、过滤、洗涤、干燥
C.蒸发浓缩至大量晶体析出后停止加热,冷却、过滤、洗涤、干燥
(4)为测定铜氨溶液中铜元素的含量,可采用如下方法:
i.移取500mL铜氨溶液于锥形瓶中,滴加稀H2SO4,调节溶液的pH为3-4
ⅱ.加入适当过量的KI溶液,并加入3mL0.5%淀粉溶液(![]() );
);
ⅲ.用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准液体积为5.80mL(I2+2S2O32-=2I-+S4O262-)。
①iii中滴定至终点时,溶液的颜色变化为______________。
②该铜氨溶液中铜元素的含量为______________g·mL-1(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作或叙述正确的是( )
A.向无色溶液中加入BaCl2溶液有白色沉淀出现,再加盐酸沉淀不消失,该溶液中一定含有SO42-
B.向某溶液中加入浓氢氧化钠溶液并加热,用湿润的红色石蕊试纸进行如图所示操作来检验溶液中是否存在NH4+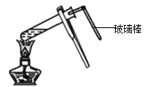
C.将某固体试样完全溶于盐酸,再滴加KSCN溶液,没有出现血红色,该固体试样中也可能存在Fe3+
D.向无色溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,则该溶液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是合成碘化物的基本原料。空气吹出法从卤水中提碘的流程如下:
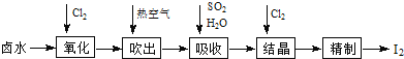
以下说法正确的是( )
A.“氧化”时,须通入过量Cl2保证I-被充分氧化
B.“吹出”操作在吹出塔中进行,应将含碘卤水从塔底进入,热空气从塔顶吹入
C.“吸收”操作中,碘蒸气与二氧化硫水溶液充分接触可生成两种酸
D.“吸收”操作中,含SO2的吸收液也可以用NaOH溶液代替,生成的I-、IO3-经酸化,即可得粗碘。使用NaOH吸收后溶液中I-、IO3-的物质的量之比为1∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示每一方框表示一种反应物或生成物,其中A、C、D、E、F在通常情况下均为气体,且加热X生成的A与C的物质的量之比为1∶1,B为常见液体。
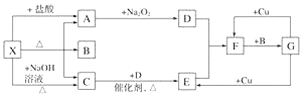
试回答下列问题:
(1)X是________(填化学式,下同),F是__________。
(2)A―→D反应的化学方程式为_______。
(3)G与Cu的反应中,G表现的性质为______。
(4)X与过量NaOH溶液反应生成C的离子方程式为_____________。
(5)以C、B、D为原料可生产G,若使amol C完全转化为G,理论上至少需要D___ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com