
分析 (1)溶于中残留固体为Fe,硝酸完全反应,Fe与硝酸反应生成Fe(NO3)2NO、NO2,未被还原的硝酸转化为Fe(NO3)2,由Fe原子守恒可知Fe(NO3)2的物质的量,被还原的硝酸转化为NO、NO2,再根据N原子守恒计算;
(2)根据N原子守恒计算HNO3的物质的量,进而计算原HNO3溶液物质的量浓度;
(3)根据总体积、电子转移守恒列方程计算各自物质的量,相同条件下物质的量比等于体积比;
(4)结合原子、电子守恒书写化学反应方程式.
解答 解:(1)溶于中残留固体为Fe,硝酸完全反应,Fe与硝酸反应生成Fe(NO3)2NO、NO2,未被还原的硝酸转化为Fe(NO3)2,
由Fe原子守恒可知n[Fe(NO3)2]=$\frac{10g-4.4g}{56g/mol}$=0.1mol,则n未被还原(HNO3)=2n[Fe(NO3)2]=0.2mol,被还原的硝酸转化为NO、NO2,n被还原(HNO3)=n(NO+)+n(NO2)=$\frac{1.792L}{22.4L/mol}$=0.08mol,故反应中被还原和未被还原的HNO3的物质的量之比为:0.08mol:0.2mol=2:5,
答:反应中被还原和未被还原的HNO3的物质的量之比为2:5;
(2)根据N原子守恒,n(HNO3)=n未被还原(HNO3)+n被还原(HNO3)=0.2mol+0.08mol=0.28mol,则原HNO3溶液物质的量浓度为$\frac{0.28mol}{0.04L}$=7mol/L,
答:原HNO3溶液物质的量浓度为7mol/L;
(3)令混合气体中NO为xmol,NO2为ymol,
则有:$\left\{\begin{array}{l}{x+y=0.08}\\{3x+y=0.1×2}\end{array}\right.$,
解得x=0.06、y=0.02
故标况下V(NO)=0.06mol×22.4L/mol=1.344L
V(NO2)=0.02mol×22.4L/mol=0.448L,
NO2和NO的体积比等于物质的量比,均为0.02mol:0.06mol=1:3,
答:NO2和NO的体积比为1:3;
(4)由上述分析可知,Fe与硝酸反应生成硝酸亚铁、NO2、NO、水,结合原子、电子守恒可知反应为5Fe+14HNO3=5Fe(NO3)2+NO2↑+3NO↑+7H2O,
答:总反应为5Fe+14HNO3=5Fe(NO3)2+NO2↑+3NO↑+7H2O.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、电子、原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| 实验步骤 | 解释或实验结论 |
| (1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)M的摩尔质量为:90g/mol. |
| (2)将此4.5g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | (2)M的分子式为:C3H6O3. |
| (3)通过M的红外光谱图发现该分子中既有羟基,还有羧基(--COOH) | (3)写出M中含有官能团羟基的电子式: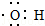 |
(4)M的核磁共振氢谱如图: | (4)M中含有4种氢原子. |
(5)综上所述,M的结构简式为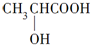 . . | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
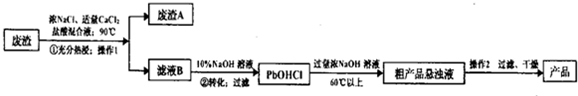
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中通过量氨气:Al3++4OH-═AlO2-+2H2O | |
| B. | 过量铁与稀硝酸反应:Fe+4H++NO3-═Fe3++NO↑+3H2O | |
| C. | 氢氧化钠溶液中通过量二氧化硫:SO2+2OH-═SO32-+H2O | |
| D. | 溴化亚铁溶液与足量氯水反应:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:X的氢化物>Y的氢化物>Z的氢化物 | |
| B. | X、Y、M三种元素可形成离子化合物 | |
| C. | 简单离子的半径:M的离子>Z的离子>Y的离子>X的离子 | |
| D. | Z元素的最高价氧化物的水化物的化学式为HZO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和乙酸 | B. | 淀粉和纤维素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙醇和二甲醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 略小于20% | B. | 略大于20% | C. | 20% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:X<Y<Z<W | B. | 单质的熔点:W>Z | ||
| C. | 热稳定性:H2Y>HX | D. | 碱性:W(OH)2>ZOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com