
【题目】砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是
A.分子中共价键键角均为60°B.黄砷中共价键键能大于白磷
C.分子中含有的共价键的数目都是4D.黄砷的熔点低于白磷
科目:高中化学 来源: 题型:
【题目】一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,则有关此电池推断正确的是( )
A.通入乙烷的电极为正极
B.参加反应的乙烷与氧气的物质的量之比为7∶2
C.放电一段时间后,KOH的物质的量浓度减少
D.负极反应式为C2H6+6H2O-14e-===2CO32-+18H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K时,各反应的平衡常数如下:
①N2(g)+O2(g)![]() 2NO(g),K=1×10-30;
2NO(g),K=1×10-30;
②2H2(g)+O2(g)![]() 2H2O(g),K=2×1081;
2H2O(g),K=2×1081;
③2CO2(g)![]() 2CO(g)+O2(g),K=4×10-92
2CO(g)+O2(g),K=4×10-92
则常温下,NO、H2O、CO2这三个化合物分解放氧的倾向最大的是( )
A.① B.② C.③ D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为V L的某密闭容器中,a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
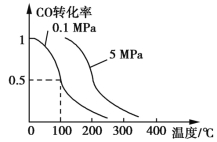
(1)该反应是 反应(填“放热”或“吸热”)。
(2)在压强为0.1 MPa条件下,200 ℃时,该反应的平衡常数K (填“=”“<”或“>”)V2/a2。
(3)在温度、容积不变的情况下,向该密闭容器再增加a mol CO(g)、2a mol H2(g)和b mol CH3OH(g),则达到新平衡时,CO的转化率 (填“增大”“减小”“不变”或“无法确定”),平衡常数 (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质反应后一定有+3价铁生成的是( )
A. 过量的Fe与Cl2反应 B. Fe与稀硝酸反应
C. FeCl3溶液中加入足量Fe粉 D. Fe和Fe2O3的混合物溶于盐酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既是化合反应又是氧化还原反应的是
A.二氧化硫催化氧化成三氧化硫:2SO2+O2![]() 2SO3
2SO3
B.氯气通入溴化钠溶液中:Cl2+2NaBr![]() 2NaCl+Br2
2NaCl+Br2
C.稀盐酸与硝酸银溶液混合反应:HCl+AgNO3![]() AgCl↓+HNO3
AgCl↓+HNO3
D.氧化钠跟水反应:Na2O+H2O![]() 2NaOH
2NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用氨水吸收烟气中的二氧化硫,其相关反应的主要热化学方程式如下: SO2(g)+NH3H2O(aq)=NH4HSO3(aq)△H1=a kJmol﹣1
NH3H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l)△H2=b kJmol﹣1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq)△H3=c kJmol﹣1
(1)反应2SO2(g)+4NH3H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的△H=kJmol﹣1 .
(2)空气氧化(NH4)2SO3的速率随温度的变化如图所示,当温度超过60℃时,(NH4)2SO3氧化速率下降的原因可能是 . 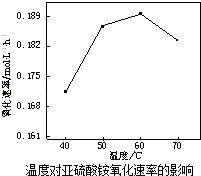
(3)以磷石膏废渣和碳酸铵为原料制备硫酸铵,不仅解决了环境问题,还使硫资源获得二次利用.反应的离子方程式为CaSO4(s)+CO32﹣(aq)SO42﹣(aq)+CaCO3(s),该反应的平衡常数K= . [已知Ksp(CaCO3)=2.9×10﹣9 , Ksp(CaSO4)=9.1×10﹣6]
(4)(NH4)2SO4在工农业生产中有多种用途. ①将黄铜精矿(主要成分Cu2S)与硫酸铵混合后在空气中进行焙烧,可转化为硫酸铜同时产生氨气.该反应的化学方程式为 .
②研究硫酸铵的分解机理有利于对磷石膏的开发.在500℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示.写出该条件下硫酸铵分解的化学方程式,并用单线桥标出电子转移的方向及数目: .
③(NH4)2SO4是工业制备K2SO4的重要原料.根据图乙中相关物质的溶解度曲线,简述工业上制备K2SO4晶体的设计思路: . 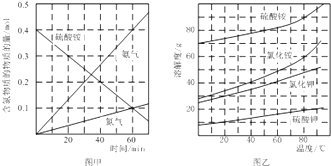
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸钠广泛用作催化剂和稳定合成剂,印染行业的还原剂,还可用于生产保险粉、草酸和甲酸.用电石炉废气(CO75%~90%,以及少量CO2、H2S、N2、CH4等),其合成部分工艺流程如下: 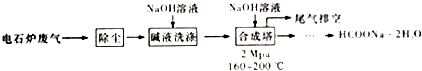
(1)上述工艺用碱液洗涤的目的是 , 可能发生的反应有(列举两利).
(2)上述合成工艺中采用循环喷射吸收合成,其目的是;最后尾气主要成分是 .
(3)合成时,得到的HCOONa溶液溶质质量分数约为5%,合成塔反应液中分离出HCOONa2H2O 的主要步骤有、、过滤,再经洗涤干燥得到.
(4)甲酸钠高温时分解制取草酸钠的化学方程式为 .
(5)在甲酸钠、氢氧化钠混合溶液中通入二氧化硫气体,可得到重要的工业产品保险粉(Na2S2O4),同时产生二氧化碳气体,该反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com