
【题目】下表是元素周期表的一部分,针对表中的a~g元素,回答下列问题:
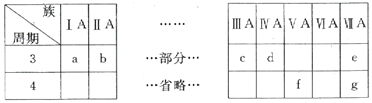
(1)d元素位于金属与非金属的分界线处,常用作__________材料。
(2)f的元素符号为As,其最高价氧化物的化学式为__________。
(3)a、b、c三种元素的最高价氧化物对应水化物的碱性逐渐减弱,试从原子结构的角度解释上述变化规律__________。
(4)e元素的非金属性强于g,请写出一个离子方程式证明:__________。
【答案】 半导体 As2O5 电子层数相同,核电荷数增加,原子半径减小,失电子能力减弱,金属性减弱 Cl2+2Br-=Br2+2Cl-
【解析】根据元素周期表的一部分可知a为钠元素,b为镁元素,c为铝元素,d为硅元素,e为氯元素,f为砷元素,g为溴元素。
(1)d为硅元素,位于金属与非金属的分界线处,常用作半导体材料;(2) As位于元素周期表第4周期ⅤA族,最外层电子数为5,所以最高正价为+5价,最高价氧化物为As2O5;(3) a为钠元素,b为镁元素,c为铝元素,位于同周期,电子层数相同,核电荷数增加,原子半径减小,失电子能力减弱,金属性减弱;(4) e为氯元素,g为溴元素,两者位于同周期,氯原子的得电子能力强于溴原子,方程式Cl2+2Br-=Br2+2Cl-可以证明。


科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.
(1)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.已知:H2(g)+Cl2(g)=2HCl(g)△H=﹣a kJmol﹣1;E(H﹣H)=b kJmol﹣1 , E(Cl﹣Cl)=c kJmol﹣1 , 则:E(H﹣Cl)=;
(2)氯原子对O3的分解有催化作用:O3(g)+Cl(g)=ClO(g)+O2(g)△H1 , ClO(g)+O(g)=Cl(g)+O2(g)△H2 , 大气臭氧层的分解反应是O3+O=2O2△H.该反应的能量变化示意图如图1所示.则反应O3(g)+O(g)=2O2(g)的正反应的活化能为kJmol﹣1 . 
(3)实验中不能直接测出由石墨和氢气反应生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧反应的反应热,求由石墨生成甲烷的反应热.已知:
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣a kJmol﹣1
②C(石墨)+O2(g)═CO2(g)△H=﹣b kJmol﹣1
③H2(g)+ ![]() O2(g)═H2O(l)△H=﹣c kJmol﹣1
O2(g)═H2O(l)△H=﹣c kJmol﹣1
则反应C(石墨)+2H2(g)→CH4(g)的反应热:
△H=kJmol﹣1 .
又已知:该反应为放热反应,△H﹣T△S可作为反应方向的判据,当△H﹣T△S<0时可自发进行;则该反应在什么条件下可自发进行 . (填“低温”、“高温”)
(4)有图2所示的装置,该装置中Cu极为极;当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铑基催化剂催化CO加氢合成甲醇(CH3OH)、乙醛(CH3CHO)、乙醇等碳的含氧化合物是近年来化学界比较活跃的研究课题之一。
(1)已知:(ⅰ)CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol
CH3OH(g) △H1=-90.1kJ/mol
(ⅱ)2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
(ⅲ)C2H5OH(g)![]() CH3OCH3(g) △H3=+50.7kJ/mol
CH3OCH3(g) △H3=+50.7kJ/mol
则由CO催化加氢制备乙醇气体(另一产物为水蒸汽)的热化学反应方程式为________。
(2)直接甲醇燃料电池(DMFC)成本低、效率高,某研究所尝试用DMFC电解处理含氰电镀废水。调节废水pHl0~12.5,电解过程中,CNˉ先被氧化成CNOˉ(两种离子中氮元素均为-3价),再进一步氧化为碳酸盐和N2。
①请写出CNOˉ被氧化的电极反应式________。
②欲处理1m3CNˉ含量为390mg/L的电镀废水,至少需准备________kg甲醇。
(3)在2.0L密闭容器中放入1 molCO与2molH2,在反应温度T1时进行如下反应:
CO(g)+2H2(g)=CH3OH(g),反应时间(t)与容器内气体总物质的量(n)的数据见下表:
时间t/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
总物质的量n/mol | 3.0 | 2.7 | 2.5 | 2.3 | 2.1 | 2.0 | 2.0 |
①在0~5min时段,反应速率v(CH3OH)为________;有利于提高上述反应平衡转化率的条件是________。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
②计算温度T1时反应的平衡常数K1________;T1时达平衡后,改变反应温度为T2,平衡常数增大,则T2________T1(填“大于”“小于”),判断理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙烯在一定条件下能发生下列转化,回答下列问题:

(1)反应①的反应类型是__________;物质C中所含官能团的名称是__________。
(2)分别写出②、④反应的化学方程式(有机物用结构简式表示):__________、__________。
(3)实验室制取乙酸乙酯的装置如下图所示。能完成本实验的装置是__________(填“甲”、“乙”或“丙”),试管B内盛放的液体是__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合H+ + OH-=H2O离子反应的是( )
A.稀硫酸与稀氨水B.稀硫酸与氢氧化钡溶液
C.稀硝酸与氢氧化钡溶液D.盐酸与氢氧化铁反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g) + 3H2(g) ![]() 2NH3(g),△H<0,在673 K,30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示,叙述正确的是( )
2NH3(g),△H<0,在673 K,30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示,叙述正确的是( )

A.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
B.点c处反应达到平衡
C.点a的正反应速率比点b的大
D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是( )
A.晶体硅可用于制造光导纤维
B.氯氧化钠用来治疗胃酸过多
C.铝制容器可以用来贮运稀硝酸
D.乙烯用作水果的催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某工厂利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬的流程:

请回答下列问题:
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
(1)在浸出过程中除生成Cr2(SO4)3外,主要还生成__________________。
(2)流程中“第一次调节“pH”是为了除去Fe3+,所加试剂X可以是_______(任写一种)。当离子浓度小于或等于1×10-5时可认为沉淀完全,若要使Fe3+完全沉淀,则应调节溶液pH≥__________已知(Ksp[Fe(OH)3]=8×10-38,1g2=0.3)
(3)写出还原步骤中生成Cu2O沉淀反应的离子方程式______________________________。此步骤中若NaHSO3过量。除了浪费试剂外,还可能出现的问题是________________________。
(4)流程中“第二次调节pH”应小于9,因为Cr(OH)3是两性氢氧化物,试写出Cr(OH)3与NaOH溶液反应的离子方程式___________________________。
(5)Cr(OH)3受热分解为Cr2O3,再用铝热法可以得到金属Cr。写出其中用铝热法冶炼得到金属Cr的化学方程式________________________________。
(6)化学需氧量(COD)可量度水体受有机物污染的程度,以K2Cr2O7作强氧化剂处理水样时所消耗的K2Cr2O7的量换算成相当于O2的含量(以mg·L-1计)来计量。
①处理时,水样应先酸化,最好选用__________(选填“稀硝酸”、“稀硫酸”或“稀盐酸”)酸化。
②在该条件下,Cr2O72-最终转化为Cr3+、取水样100mL,处理该水样时消耗了10mL0.025 mol·L-1 K2Cr2O7溶液。则该水样的COD为__________ mg·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com