
分析 X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol•L-1、0.6mol•L-1、0.2mol•L-1,利用极值转化分析各物质的浓度取值范围.
解答 解:设X转化的浓度为x,
X(g)+3Y(g)?2Z(g)
初始:c1 c2 c3
平衡:0.1moL/L 0.6mol/L 0.2mol/L
极值转化(正向) 0 0.3mol/L 0.4mol/L
极值转化(逆向) 0.2mol/L 0.9mol/L 0
反应为可逆反应,物质不可能完全转化,c1、c2、c3的范围分别为:0<c1<0.2、0.3<c2<0.9、0<c3 <0.4;
故答案为:0<c1<0.2;0.3<c2<0.9;0<c3 <0.4.
点评 本题考查化学平衡的计算,题目难度不大,本题注意化学平衡状态的判断方法以及可逆反应的特点.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:多选题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:4 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 此有机物的最简式为CH4O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图1所示装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. | 图2所示装置用于除去碳酸氢钠固体中的少量碳酸钠 | |
| C. | 图3所示装置配制100mL0.1mol•L-1的硫酸 | |
| D. | 图4所示装置用于分离出溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种 | |
| B. | C8H10中只有三种属于芳香烃的同分异构体 | |
| C. | C5H10中只有三种属于直链烯烃的同分异构体(包括空间异构) | |
| D. | 含两个-COOCH3的有机物(C7H12O4)属于酯的同分异构体多于4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
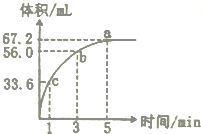 某“学习小组”研究影响化学反应速率的因素.向10 mL某浓度的H2O2溶解中加入一定量MnO2粉末,在标准状况下放出气体的体积和时间的关系如图所示,
某“学习小组”研究影响化学反应速率的因素.向10 mL某浓度的H2O2溶解中加入一定量MnO2粉末,在标准状况下放出气体的体积和时间的关系如图所示,查看答案和解析>>
科目:高中化学 来源: 题型:填空题
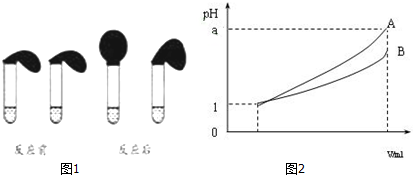
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
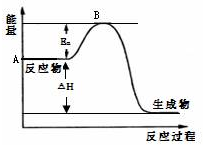 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1molSO2(g)完全转化为1molSO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1molSO2(g)完全转化为1molSO3(g)放热99kJ.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
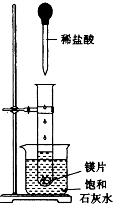 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 有机物一定含C,H元素,可能含氧元素 | |
| B. | 有机物只含C,H元素 | |
| C. | 有机物含C,H,O元素 | |
| D. | 此有机物化学式为CH4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com