
| A. | 只有AgBr沉淀生成 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | AgCl沉淀多于AgBr沉淀 |
分析 向AgCl与 AgBr的饱和溶液中,加入AgNO3,AgCl与AgBr的溶解平衡向左移动,但AgBr的溶解度更小,溶液中AgCl沉淀较多.
解答 解:在AgCl和AgBr两饱和溶液中,前者c(Ag+)大于后者c(Ag+),c(Cl-)>c(Br-),当将AgCl、AgBr两饱和溶液混合时,发生沉淀的转化,生成更多的AgBr沉淀,与此同时,溶液中n(Cl-)比原来AgCl饱和溶液中大,当加入足量的浓AgNO3溶液时,AgBr沉淀有所增多,但AgCl沉淀增加更多,
故选D.
点评 本题考查难溶电解质的溶解平衡,为高频考点,解答本题时注意AgCl的溶解度比AgBr大,加入硝酸银,抑制溶解平衡向右移动,生成沉淀更多,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | N2是还原产物,且还原剂与氧化剂物质的量之比是2:3 | |
| B. | N2是氧化产物,且还原剂与氧化剂物质的量之比是2:3 | |
| C. | 每转移6mol电子就生成22.4LN2 | |
| D. | NH4Cl是氧化产物,且还原产物与氧化产物物质的量之比是1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl沉淀生成和溶解不断进行,但速率相等 | |
| B. | AgCl难溶于水,溶液中没有Ag+和Cl- | |
| C. | 其他条件不变时,加水可使Ksp(AgCl)增大 | |
| D. | 向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
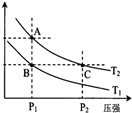 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl不能转化为AgI | |
| B. | 25℃时,0.1mol/L HF溶液pH=l | |
| C. | 25℃时,使AgCl转化为AgI,则加入KI溶液的浓度不低于5×10-12mol/L | |
| D. | 向1L0.1mol/LHF溶液中加入1L 0.1mol/LCaCl2溶液,没有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池放电时,电池负极周围溶液的pH 不断增大 | |
| B. | 电池充电时,阳极反应为:Ni(OH)2+OH--e-═NiO(OH)+H2O | |
| C. | 电池充电时,氢元素被氧化 | |
| D. | 电池放电时,负极反应为:H2-2e-═2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 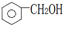 醇类-OH 醇类-OH | B. | CH3CH2COOH 羧酸类-COOH | ||
| C. | 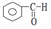 酮类-CHO 酮类-CHO | D. | CH3CH2Br 卤代烃类-Br |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com