
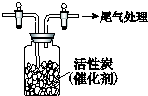
 ijѧϰС������SO2���л�ԭ�ԣ��Ʋ�SO2�ܱ�Cl2��������SO2Cl2��
ijѧϰС������SO2���л�ԭ�ԣ��Ʋ�SO2�ܱ�Cl2��������SO2Cl2������ I�������ڻ������У�Ԫ�ػ��ϼ۵Ĵ�����Ϊ����н��
�������̺�Ũ���ᷴӦ�����������Ȼ��̺�ˮ��
��Ũ���������ˮ�ԣ����Ը���������
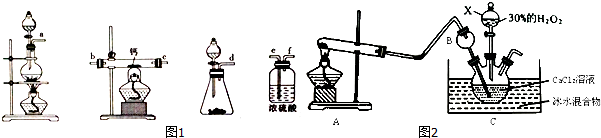
������1����SO2Cl2��H2O��Ӧ����������Ȼ��⣻
���������������ӷ�Ӧ���ɲ���Һ������Ȼ���������ע��Ӧ�ȼ������ᱵ��Һ�����ų���������ӵĸ��ţ�
��2��SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��SO2Cl2�ֽ�õ��������Ͷ���������ˮ��Һ�з���������ԭ��Ӧ����������Ȼ��⣬�������Ȼ�����Ӧ�������ᱵ������
��� �⣺I��SO2Cl2�У���Ϊ-2�ۣ���Ϊ-1�ۣ������ڻ������У�Ԫ�ػ��ϼ۵Ĵ�����Ϊ���֪��Ԫ�ػ��ϼ�Ϊ+6�ۣ�
�ʴ�Ϊ��+6�ۣ�
II���������̺�Ũ���ᷴӦ�ķ���ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��Ҫ�ռ����������Ӧ��ȥ�����е�ˮ������ѡ��Ũ������Ը���������
�ʴ�Ϊ��Ũ���
������1��SO2Cl2��ˮ��Ӧ�ķ���ʽ����SO2Cl2+2H2O=H2SO4+2HCl��
�ʴ�Ϊ��SO2Cl2+2H2O=H2SO4+2HCl��
��Ҫ������Һ�е�������Ӧ�ų���������ӵĸ��ţ����ԣ�ȡ��������Һ���Թ��У��������Ba��NO3��2��Һ�����ˣ�����Һ�еμ�HNO3�ữ���ټ���AgNO3��Һ����������ɫ��������˵����Һ����Cl-��
�ʴ�Ϊ��ȡ��������Һ���Թ��У��������Ba��NO3��2��Һ�����ˣ�����Һ�еμ�HNO3�ữ���ټ���AgNO3��Һ����������ɫ��������˵����Һ����Cl-��
��2��SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��SO2Cl2�ֽ�õ��������Ͷ���������ˮ��Һ�з���������ԭ��Ӧ����������Ȼ��⣬�������Ȼ�����Ӧ�������ᱵ������
�ʴ�Ϊ��BaSO4��
��SO2��Cl2��Ӧ�Ļ�ѧ����ʽΪ��SO2+Cl2=SO2Cl2�����ڰ�ɫ������BaSO4�����Է�Ӧ��Ļ�������б�Ȼ����SO2��Cl2�������壮���SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��
�ʴ�Ϊ��SO2+Cl2=SO2Cl2�����ڰ�ɫ������BaSO4�����Է�Ӧ��Ļ�������б�Ȼ����SO2��Cl2�������壮���SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��
���� ���⿼�����ʷ�������ƣ���Ŀ�Ѷ��еȣ���ȷ���ʵ������ǽ���ؼ���ע�����ճ������Ӽ���ķ�������ѧ����ʽ����дԭ������������ѧ���ķ�����������ѧʵ��������


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
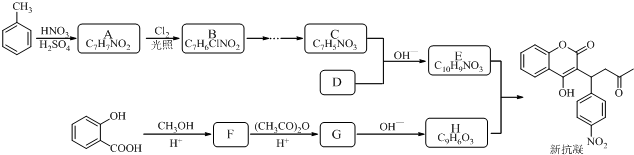
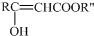
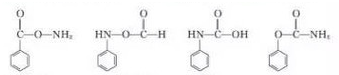
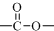 �ṹ��
�ṹ��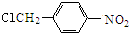 $��_{��}^{NaOHˮ��Һ}$
$��_{��}^{NaOHˮ��Һ}$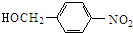 $��_{����}^{O_{2}}$
$��_{����}^{O_{2}}$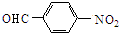
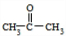 ��E
��E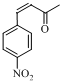
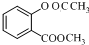 $\stackrel{OH-}{��}$
$\stackrel{OH-}{��}$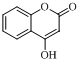 +CH3OH��
+CH3OH���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HBr��KOH��CaCO3��H2O����ǿ����� | |
| B�� | Na2O2��CaO��Al2O3���Ǽ��������SiO2��SO2��NO2�������������� | |
| C�� | 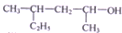 ������Ϊ4-��-2-���� ������Ϊ4-��-2-���� | |
| D�� | ${\;}_{94}^{238}$Pu��������Ϊ94��������Ϊ238��������Ϊ144 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ���� |
| ��ʢ��4g CaO2�Ĵ��Թ��м���10mLϡ�������Һa | ���ҷ�Ӧ��������ʹ������ľ����ȼ������ |
| ȡ5mL��Һa���Թ��У���������ʯ�� | ��Һ��죬һ��ʱ�����Һ��ɫ���Ա�dz���Ժ���Һ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£�0.2mol•L-1��һԪ��BOH���Ũ�ȵ�����������Ϻ�������Һ�в���������ּ�Ũ����ͼ��ʾ�����жԻ����Һ�ķ�����ȷ���ǣ�������
�����£�0.2mol•L-1��һԪ��BOH���Ũ�ȵ�����������Ϻ�������Һ�в���������ּ�Ũ����ͼ��ʾ�����жԻ����Һ�ķ�����ȷ���ǣ�������| A�� | ��Һ���������Ի����� | B�� | ���£�c��X������c��Y����С | ||
| C�� | c��B+��+c��Y��=c��Cl-�� | D�� | ϡ����Һ��c��X������c��Z������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��ֻ����2�ֻ�����ķ��� | |
| B�� | ͨ��CO2ʱ��Һ��Ư�����ü��� | |
| C�� | ����Һ��A13+��Fe2+��SO42-��NO3-���Դ������� | |
| D�� | ��SO2��Ӧ�����ӷ���ʽΪCa2++2ClO-+SO2+H2O=CaSO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2�����ڼӹ�ʳƷ��ʹʳƷ���� | |
| B�� | NaOH��������ϴ�����̻� | |
| C�� | �����ǿ����ںϳɱ���ҩ��ά����C | |
| D�� | �۱�ϩ���Ͽ�����ʳƷ����Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
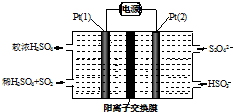 ��ҵβ��SO2�ж������պʹ���������
��ҵβ��SO2�ж������պʹ����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ֧�Թ���ֻ����������һ֧�Թ�������������ʱ����μӵ���AlCl3��Һ | |
| B�� | ��һ֧�Թ���ֻ����������һ֧�Թ�������������ʱ����μӵ���H2SO4 | |
| C�� | ����֧�Թ��ж�ֻ������ɫ����ʱ����μӵ���Ba��0H��2��Һ | |
| D�� | ����֧�Թ��мȲ��������ֳ�������ʱ����μӵ���NH4HCO3��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com