
(14分)短周期主族元素A、B、C、D、E原子序数依次增大 , A是元素周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物分子含有相同的电子数。
⑴A、C、D形成的化合物中含有的化学键类型为 。
⑵已知:
① E-E→2E ?H=+a kJ/mol;
② 2A→A-A ?H=-b kJ/mol;
③ E+A→A-E ?H=-c kJ/mol;
写出298K时,A2与E2反应的热化学方程式 。
⑶在某温度下容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g) ?H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g) ?H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
平衡时n(X) | 0.5 mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 |
|
|
|
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则A2的平均反应速率
v (A2)= 。
② 计算该温度下此反应的平衡常数K = 。
③三个容器中的反应分别达平衡时下列各组数据关系正确的是 (填字母)。
A.α1+α2=1 B.Q1+Q2=Q C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0 mol F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体积压缩到1 L,若在第8min达到新的平衡时A2的总转化率为75%,请在下图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。

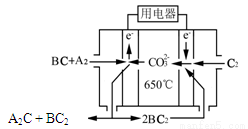
⑷熔融碳酸盐燃料电池(MCFC)是一种高温燃料电池,被称为第二代燃料电池,是未来民用发电的理想选择方案之一,其工作原理如图所示。现以A2(g)、BC(g)为燃料,以一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出该碳酸盐燃料电池(MCFC)正极的电极反应式____________________________。
⑴ 离子键、极性键(或共价键)
⑵ H2(g)+Cl2(g)=2HCl(g) ?H=(a+b-2c)kJ·mol-1[?H表示成-(2c-a-b)kJ·mol-1也可]
⑶ ① 0.125 mol·L-1·min-1
② 4 L2/mol2 ③ ABD
④

⑷ O2+4e-+2CO2=2CO32 -
【解析】
试题分析:根据题意依次推出A为氢元素,B为碳元素,C为氧元素,D为钠元素,E为氯元素;
⑴A、C、D形成的化合物为NaOH,其所含化学键为离子键、极性键(或共价键);
⑵首先写出A2与E2反应的方程式,并标出各物质的状态为H2(g)+Cl2(g)=2HCl(g);将“①-②+③×2”得该化学方程式,根据盖斯定律得该反应热?H=(a+b-2c)kJ·mol-1,据此便可写出完整的热化学方程式;
⑶①A2的平均反应速率v (A2)=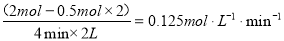 ;
;
②该温度下此反应的平衡常数K= ;
;
③甲和乙两容器的平衡状态为全等平衡,则有α1+α2=1,Q1+Q2=Q,P1=P2,n2=n1=0.5 mol;由于丙容器的起始量是甲的2倍,可将丙容器的体积扩大2倍(与甲同压等效),然后再恢复到原体积,则可得α3>α1,P3<2P1,n2<1.0 mol<n3,Q3>2Q1,综上只有A、B、D项正确。
④第5min时X的物质的量浓度变为0.5 mol/L(体积变为1 L),再根据“第8min达到新的平衡时A2的总转化率为75%”,则到新平衡时X的物质的量浓度为 ,据此便可作图。
,据此便可作图。
⑷O2在正极上发生还原反应生成CO32 -:O2+4e-+2CO2=2CO32 -。
考点:本题考查化学与热量、化学反应速率与化学平衡常数、等效平衡、电化学等。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
用铅蓄电池电解甲、乙电解池中的溶液。 电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )
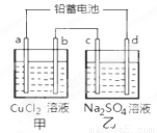
A.d极为阴极
B.若利用甲池精炼铜,b极应为粗铜
C.放电时铅蓄电池负极的电极反应式为:
PbO2(s) + 4 H+(aq)+SO4 2-(aq)+4e- = PbSO4 (s) +2H2O (l)
D.若四个电极材料均为石墨,当析出6.4 g Cu时,两池中共产生气体3.36 L(标准状况下)
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
化学在人类生活中扮演着重要角色,以下应用不正确的是( )
A.用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的
B.福尔马林是一种良好的杀菌剂,能用来消毒饮用水
C.医疗上常用体积分数为70%~75%的酒精作消毒剂
D.为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因
B.CH4、NH3、PH3的热稳定性逐渐增强
C.因为酸性:HC1>HF,所以非金属性:Cl>F
D.钠原子在反应中失去的电子比铝原子少,故钠的金属性比铝弱
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
下图是某煤发电厂处理废气的装置示意图。下列说法错误的是( )

A.使用此废气处理装置可减少酸雨的形成
B.装置内发生的反应有化合、分解、置换和氧化还原反应
C.整个过程的反应可表示为2SO2+2CaCO3+O2=2CaSO4+2CO2
D.可用酸性高锰酸钾溶液检验废气处理是否达标
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三终极预测理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法错误的是
A.一定条件下,2 mol SO2和1 mol O2混合在密闭容器中充分反应后容器中的分子数大于2NA
B.256 g S8分子中含S-S键为7NA个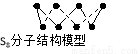
C.由1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个
D.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)在温度t℃下,某Ba(OH)2的稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,向该溶液中逐滴加入pH=b的NaHSO4,测得混合溶液的部分pH如下表所示:
序号 | 氢氧化钡的体积/mL | 硫酸氢钠的体积/mL | 溶液的pH |
① | 33.00 | 0.00 | 8 |
② | 33.00 | x | 7 |
③ | 33.00 | 33.00 | 6 |
(1)依据题意判断,t℃___________25℃(填“大于”、“小于”或“等于”),该温度下水的离子积常数Kw = ___________。
(2)b=____________,x = ______mL 。
(3)反应③的离子方程式为____________________________
(4)将此温度下的Ba(OH)2溶液取出1mL,加水稀释至1L,则稀释后溶液中
c(Ba2+)﹕c(OH-)= ;
(5) 与NaHSO4相同, NaHSO3 和NaHCO3也为酸式盐。已知NaHSO3溶液呈酸性,NaHCO3溶液呈碱性。现有浓度均为0.1mol/L的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中可能正确的是___________(填正确答案的标号)。
A.c( )>c(
)>c( )>c(
)>c(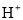 )>c(
)>c( )>c(
)>c( )
)
B.c( )+c(
)+c(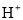 )=c(
)=c( )+2c(
)+2c( )+c(
)+c( )
)
C.c(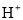 )+c(
)+c( )=c(
)=c( )+c(
)+c( )
)
D.两溶液中c( )、c(
)、c( )、c(
)、c( )分别相等
)分别相等
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是

A.1 mol该物质能与3molH2发生加成反应
B.1 mol该物质最多可与2 mol NaOH反应
C.分子中含醇羟基,能被酸性KMnO4溶液氧化为乙酸
D.该物质不能聚合为高分子化合物
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
工业上获得苯主要通过( )
A.煤的干馏 B.石油常压分馏 C.石油减压分馏 D.石油催化裂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com