
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
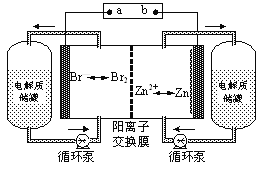
A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学设计实验制备并探究SO2的性质。回答下列问题:
(1)实验室用废铜屑制备SO2的化学方程式为______。
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有______性。
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为______。
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为______。(Cr2O72-被还原为Cr3+)
(5)常温下,改变0.1molL-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=  ]随pH的变化如图所示:
]随pH的变化如图所示:

H2SO3的lgKa1=______;反应HSO3-+OH-![]() SO32-+H2O的lgK=______;用0.100molL-1NaOH溶液滴入0.100molL-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______。
SO32-+H2O的lgK=______;用0.100molL-1NaOH溶液滴入0.100molL-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1mol/LNH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发)。下列说法不正确的是
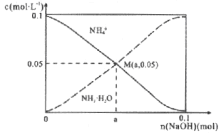
A. M点溶液中水的电离程度比原溶液小
B. 在M点时,n(OH-)-n(H+)=(a-0.05)mol
C. 随着NaOH的加入, 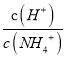 不断增大
不断增大
D. 当n(Na0H)=0.1mol时,c(Na+)=c(NH4+)+c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、技术、社会发展息息相关。下列说法不正确的是( )
A.食醋除水垢、油脂的皂化、煤的干馏都是化学变化
B.侯氏制碱法的工艺过程中应用了物质溶解度的差异
C.黑火药是我国古代的四大发明之一,配方为“一硫二硝三木炭”,其中的硝指的是硝酸
D.“绿水青山就是金山银山”,矿物燃料经过脱硫脱硝处理,可减少![]() 、
、![]() 的排放
的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用Pt电极电解1 L浓度均为0.1 mol·L-1的HCl、CuSO4的混合溶液,装置如图,下列说法正确的是( )

A.电解开始时阴极有H2放出
B.电解开始时阳极上发生:Cu2++2e-Cu
C.整个电解过程中,SO42-不参与电极反应
D.当电路中通过电子的量超过0.1 mol时,此时阴极放电的离子发生了变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1830年,瑞典化学家塞弗斯托姆从一种铁矿石中得到了一种新元素,并以凡娜迪丝女神(![]() )之名命名为“钒”。钒(
)之名命名为“钒”。钒(![]() )的用途很广,在冶金行业有“第一金属”的美誉。
)的用途很广,在冶金行业有“第一金属”的美誉。
(1)基态钒原子能量最高的电子占据的能级符号为_________。
(2)依据价电子互斥理论推测![]() 的立体构型是______________。
的立体构型是______________。
(3)①化合物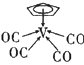 中,中心原子V的价电子与配体提供的电子数之和为18,配体
中,中心原子V的价电子与配体提供的电子数之和为18,配体![]() 不带电荷,且其提供的是大π键的电子,则配体“
不带电荷,且其提供的是大π键的电子,则配体“![]() ”中的大π键可表示为_______。(例如苯中大π键可表示为
”中的大π键可表示为_______。(例如苯中大π键可表示为![]() )
)
②从电负性角度解释![]() 作配体时,配位原子是C而不是O的原因是___________________。
作配体时,配位原子是C而不是O的原因是___________________。
(4)2-巯基烟酸氧钒配合物(如图甲)是有效调节血糖的新型药物的主要成分。
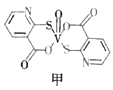
①2-巯基烟酸氧钒配合物中![]() 键长_________(填“大于”“等于”或“小于”)V—O键长,该物质中氮原子的杂化方式是_________________。
键长_________(填“大于”“等于”或“小于”)V—O键长,该物质中氮原子的杂化方式是_________________。
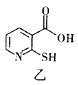
②相同条件下,2-巯基烟酸(如图乙)在水中溶解性好于2-巯基烟酸氧钒配合物的原因是____。
(5)某钒的氧化物的晶胞如图。
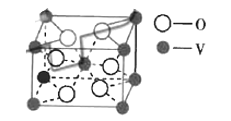
①氧的配位数为_____________。
②已知上述晶胞为立方晶胞,距离最近的钒原子和氧原子间的核间距为![]() ,晶体密度为
,晶体密度为![]() ,则晶胞中底面上的两个氧原子的核间距为__________cm.
,则晶胞中底面上的两个氧原子的核间距为__________cm.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计了一系列实验,根据具体实验回答下列问题:
Ⅰ.制取![]()
化学反应方程式为![]() 。
。
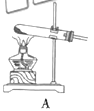
(1)根据实验需要,下列![]() 装置中___________(填序号)最适合制备
装置中___________(填序号)最适合制备![]() 。
。
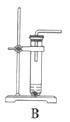
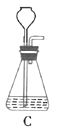

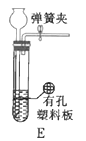
(2)在实验中发现,![]() 气体产生缓慢,但又不存在气密性问题,分析可能的原因:____________、_________________。(任写两条)
气体产生缓慢,但又不存在气密性问题,分析可能的原因:____________、_________________。(任写两条)
Ⅱ.制取![]() 、
、![]() 混合气体并验证(实验装置如图所示)
混合气体并验证(实验装置如图所示)
化学反应方程式为![]() 。
。
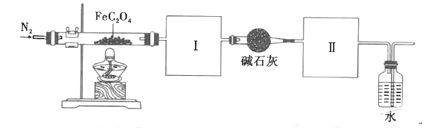
(3)根据实验需要,请从下列![]() 装置中选择最适合的装置并将其序号填在下面的空格中:Ⅰ、Ⅱ处连接的装置分别是________________、________________。上图中装水的洗气瓶的作用是___________。
装置中选择最适合的装置并将其序号填在下面的空格中:Ⅰ、Ⅱ处连接的装置分别是________________、________________。上图中装水的洗气瓶的作用是___________。
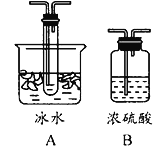
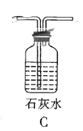
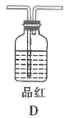
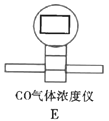
Ⅲ.测定样品中![]() 的含量
的含量
(4)某草酸亚铁样品中含有少量硫酸亚铁,设计用滴定法测定该样品中![]() 的含量,滴定反应为
的含量,滴定反应为![]() 。
。
实验方案设计如下:
①将准确称量的ag草酸亚铁样品置于![]() 锥形瓶内,加入适量
锥形瓶内,加入适量![]() 的
的![]() 溶解,加热至70℃左右,立即用浓度为
溶解,加热至70℃左右,立即用浓度为![]() 的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液
的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液![]() 。
。
②向上述滴定混合液中加入适量的![]() 粉和过量的
粉和过量的![]() 的
的![]() 溶液,煮沸(不含
溶液,煮沸(不含![]() ),继续用
),继续用![]() 的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液
的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液![]() 。回答下列问题:
。回答下列问题:
步骤②中检验溶液不含![]() 的操作为取1滴煮沸后的溶液滴入装有___________________溶液的试管中,若_______,则说明溶液不含
的操作为取1滴煮沸后的溶液滴入装有___________________溶液的试管中,若_______,则说明溶液不含![]() 。计算
。计算![]() (
(![]() 的摩尔质量为
的摩尔质量为![]() )的质量分数为__________%。(用含
)的质量分数为__________%。(用含![]() 的式子表示)
的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班学生通过分组实验测定酸碱滴定曲线。
实验用品:0.1 mol·L-1HCl溶液、0.1 mol·L-1NaOH溶液、蒸馏水、pH计、酸式滴定管、碱式滴定管、铁架台(带滴定管夹)、锥形瓶。甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00 mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,其中乙和丙两组同学的操作上都存在着不足或失误。
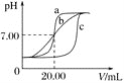
请回答下列问题:
(1)实验前pH计应用标准溶液进行校准,若将pH计放入c(H+)=0.0001 mol·L-1的标准溶液中校准,则pH计的读数应为________。
(2)甲组同学滴定时选用的滴定管为________(填“酸式”或“碱式”)滴定管,最后一次润洗滴定管应选用实验用品中的________进行润洗。
(3)乙组同学操作上的不足之处是________________________________________。
(4)造成丙组同学的曲线与甲组同学不同的原因可能是________(填字母)。
A.用待装液润洗锥形瓶
B.滴定使用的滴定管的尖嘴部分在滴定前有气泡未排出,滴定后气泡消失
C.滴定前后对滴定管进行读数的视线分别如图所示

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。下列说法不正确的是
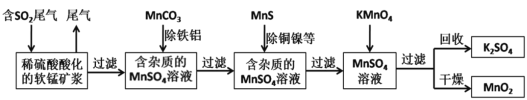
A.上述流程中多次涉及到过滤操作,实验室进行过滤操作时需用到的硅酸盐材质仪器有:玻璃棒、烧杯、漏斗
B.用MnCO3能除去溶液中的Al3+和Fe3+,其原因是MnCO3消耗了溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀
C.实验室用一定量的NaOH溶液和酚酞试液就可以准确测定燃煤尾气中的SO2含量
D.MnSO4溶液→MnO2过程中,应控制溶液pH不能太小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com