
【题目】现有A、B、C三种化合物,各取40g相混合,完全反应后,容器中只有18gB、49gC,还有D生成,已知D的相对分子质量为106。下列说法中不正确的是( )
A.化学方程式一定是A+B=C+D
B.生成D的物质的量为0.5mol
C.若化学方程式为2A+B=C+D,则A的摩尔质量为40g·mol-1
D.若D是碳酸钠,则钠离子的质量为23g
【答案】A
【解析】
现有A、B、C三种化合物,各取40g相混合,完全反应后,容器中只有18gB、49gC,还有D生成,则40gA完全反应,参加反应的B的质量为40g-18g=22g,生成的C的质量为49g-40g=9g,根据质量守恒定律反应生成的D的质量为40g+22g-9g=53g。
A.由分析知A和B是反应物,C和D是生成物,但无法确定A、B、C、D的物质的量之比,即反应方程式不一定为A+B=C+D,故A错误;
B.反应生成的D的质量为53g,D的相对分子质量为106,则生成D的物质的量为![]() =0.5mol,故B正确;
=0.5mol,故B正确;
C.若化学方程式为2A+B=C+D,结合D的物质的量为0.5mol,则A的物质的量为1mol,其的摩尔质量为![]() =40g·mol-1,故C正确;
=40g·mol-1,故C正确;
D.若D是碳酸钠,物质的量为0.5mol,则钠离子的物质的量为1mol,质量为23g,故D正确;
故答案为A。


科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是
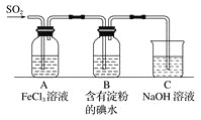
A. 能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
B. 装置C的作用是吸收SO2尾气,防止污染空气
C. 为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去
D. 为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1KOH溶液滴定10.00mL0.10mol·L-1H2C2O4(二元弱酸)溶,所得滴定曲线如图所示(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是( )
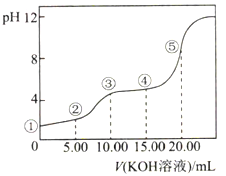
A. 点①所示溶液中:c(H+)/c(OH-)=1012
B. 点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
C. 点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. 点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+ c(C2O42-)=0.10mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)=2C(g)+D(g),经2min,B的浓度减少0.6 molL-1。对此反应速率的表示正确的是( )
①用A表示的反应速率是0.4 molL-1min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 molL-1min-1
④在这2 min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的
A. ①②
B. ③
C. ①
D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲在高端、尖端科技产业日显重要。工业上开发铜阳极泥[主要成分碲化亚铜(Cu2Te),少量Ag、Au]回收碲,其工业流程如下:

(1)碲是ⅥA族元素,Cu2Te中碲元素的化合价为_______________。
(2)“氧化酸浸”中加入足量H2O2的作用是______________。
(3)“滤液②”中主要阴离子是_______________。
(4)“还原”阶段,理论上得到1 mol Te,则消耗_________mol Na2SO3。
(5)CuC2O4分解的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.3mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(1)如图所示,配制上述溶液还需用到的玻璃仪器是__(填仪器名称)。
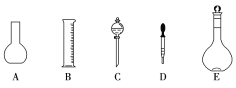
(2)下列操作中,容量瓶所不具备的功能有___(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(3)根据计算,用托盘天平称取NaOH的质量为___g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___(填“偏大”“不变”或“偏小,下同)。若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 当H2O与Na2O2反应生成1molO2时,转移的电子数目为2×6.02×1023
B. 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C. 常温下2S2O(g)![]() 3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应
3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应
D. 氯水通入SO2后溶液的酸性减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com