
| A. |  | B. |  | ||
| C. |  | D. |  |
分析 该反应的△H=+50.5kJ•mol-1,为吸热反应,反应物总能量小于生成物总能量,活化能Ea=90.4kJ•mol-1.焓变等于正逆反应的活化能之差,以此来解答.
解答 解:该反应的△H=+50.5kJ•mol-1,为吸热反应,反应物总能量小于生成物总能量,B、C均为放热反应,排除选项BC;
活化能Ea=90.4kJ•mol-1,焓变等于正逆反应的活化能之差,逆反应的活化能=Ea-△H=39.9kJ•mol-1,A中Ea与△H的比例不满足,而能量关系图D合理,
故选D.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变与活化能判断为解答的关键,侧重分析与应用能力的考查,选项A为解答的易错点,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯的链节为-CH2- | |
| B. | 丙烷的二氯代物有4种 | |
| C. | 甲苯在溴化铁作催化剂与液溴发生反应,一溴代物只有一种 | |
| D. | CH3CH═CH2在一定条件下与HCl加成产物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子的氧化性由强到弱的顺序为:Br->I->S2- | |
| B. | 离子的还原性由强到弱的顺序为:S2->I->S2- | |
| C. | 元素的非金属性由强到弱的顺序为:S>I>Br | |
| D. | 单质的氧化性由强到弱的顺序为:Br2>I2>S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4的电极为负极 | |
| B. | 正极反应为:2O2+4H2O+8e-═8OH- | |
| C. | 燃料电池工作时,溶液中的OH-向正极移动 | |
| D. | 该电池使用一段时间后溶液中KOH的浓度将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量的Cu与含有0.2molH2SO4的浓硫酸共热可生成SO2为0.1NA | |
| B. | 标准状况下,22.4LCCl4中含有的分子数目为NA | |
| C. | 7.8gNa2S和Na2O2的混合物中,含有的阴离子数目为0.1NA | |
| D. | 标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为 0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ③金刚石 ④35Cl ⑤
③金刚石 ④35Cl ⑤
 ⑦
⑦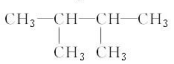 ⑧氯气 ⑨石墨 ⑩37Cl
⑧氯气 ⑨石墨 ⑩37Cl
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com