
| A. | HCHO与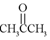 | B. | HOCH2CH3与CH3COOH | ||
| C. | HCOOH与C5H11COOH | D. | C2H4与C3H6 |
分析 结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物,同系物必须是同一类物质(含有相同且数量相等的官能团).
解答 解:A、HCHO是甲醛,属于醛类,而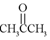 是丙酮,属于酮类,两者的官能团不同,结构不相似,故不是同系物,故A错误;
是丙酮,属于酮类,两者的官能团不同,结构不相似,故不是同系物,故A错误;
B、HOCH2CH3是乙醇,而CH3COOH是乙酸,两者的官能团不同,结构不相似,故不是同系物,故B错误;
C、HCOOH与C5H11COOH均属于羧酸类,结构相似,分子组成相差5个“CH2”原子团,故互为同系物,故C正确;
D、C2H4一定是乙烯,属于烯烃,但C3H6不一定是丙烯,还可能为环丙烷,故两者不一定是同系物,故D错误.
故选C.
点评 本题考查了同系物的判断,题目难度不大,注意掌握同系物的概念及判断方法,明确互为同系物的化合物一定满足结构相似,即含有的官能团类型及数目一定相同.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸滴入胆矾中,胆矾失水变白,发生了化学变化 | |
| B. | 二氧化硫能使溴水褪色,体现二氧化硫的漂白性 | |
| C. | 浓硫酸与灼热的木炭反应,体现浓硫酸的强氧化性和酸性 | |
| D. | 加热时硫与铜反应生成黑色的硫化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴入盐酸,有无色无味的气体产生,说明某溶液一定含有含CO32- | |
| B. | 向某溶液中加入NaOH溶液,并加热,产生的气体能使湿润的红色石蕊试纸变蓝,说明某溶液中一定含有NH4+ | |
| C. | 向某溶液中滴加氯化钡溶液,得到白色沉淀,说明某溶液中一定含有SO42- | |
| D. | 向某溶液中加入过量的NaOH溶液的白色沉淀,又观察到颜色逐渐变为红褐色说明某溶液中一定含有Fe2+,一定不含有Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释溶液,$\frac{c(HC{O}_{3}^{-}C)•c(O{H}^{-})}{c(C{O}_{3}^{2-})}$不变 | |
| B. | 通入CO2,溶液pH增大 | |
| C. | 升高温度,平衡常数减小 | |
| D. | 加入NaOH固体,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、NO2、CO、烟尘 | B. | HCl、SO2、N2、粉尘 | C. | NH3、CO2、NO、雾 | D. | CO2、Cl2、O2、酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁可用作红色油漆和涂料 | B. | 氧化铝可制耐高温实验材料 | ||
| C. | 明矾可用作净水剂 | D. | 用铝制餐具长时间存放碱性食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
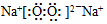 ,该化合物中的化学键类型有离子键、(非极性)共价键.
,该化合物中的化学键类型有离子键、(非极性)共价键.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com