
【题目】与NO2+互为等电子体的分子________,根据等电子体原理,在NO2+中氮原子轨道杂化类型是________;O22+与N2互为等电子体,1mol O22+中含有的π键数目为________个。
科目:高中化学 来源: 题型:
【题目】MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):
M2+(g)+CO32-(g) ![]() M2+(g)+O2(g)+CO2(g)
M2+(g)+O2(g)+CO2(g)
![]()
![]()
![]()
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A. ΔH1(MgCO3)>ΔH1(CaCO3)>0
B. ΔH2(MgCO3)=ΔH2(CaCO3)>0
C. ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO)
D. 对于MgCO3和CaCO3,ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。X、Y、Z、W最外层电子数之和为16,Y 原子的最外层电子数是其内层电子数的3倍,Z2+ 与Y2- 具有相同的电子层结构,W 与X 同主族。下列说法正确的是
A.原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.Y分别与Z、X形成的化合物中化学键类型相同
C.X的最高价氧化物对应的水化物是一种强酸
D.Y的气态简单氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:
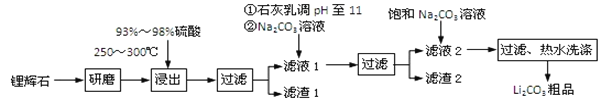
已知:
①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2 + H2SO4(浓) ![]() Li2SO4 + Al2O3·4SiO2·H2O
Li2SO4 + Al2O3·4SiO2·H2O
③某些物质的溶解度(s)如下表所示。
T/℃ | 20 | 40 | 60 | 80 |
s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣Ⅰ中分离出Al2O3的流程如下图所示。请写出生成沉淀的离子方程式______。
![]()
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)________________________________________________。
(3)最后一个步骤中,用“热水洗涤”的原因是______________________________。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是_________________________
②电解后,LiOH溶液浓度增大的原因_________________,b中生成Li2CO3反应的化学方程式是___________________________________________。
(5)磷酸亚铁锂电池总反应为:FePO4+Li![]() LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有K2Cr2O7的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有 K2Cr2O7 的废水并回收重铬酸,具体的流程如下:
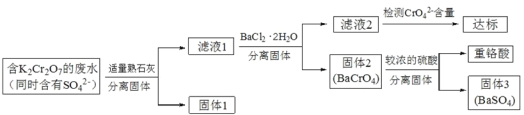
已知:CaCr2O7、BaCr2 O7 易溶于水,其它几种盐在常温下的溶度积如下表所示。
物质 | CaSO4 | CaCrO4 | BaCrO4 | BaSO4 |
溶度积 | 9.1106 | 2.30 102 | 1.17 1010 | 1.08 1010 |
(1)用离子方程式表示K2Cr2O7溶液中同时存在 K2CrO4的原因(将离子方程式补充完整):______Cr2O72-+______![]() ____CrO42+______
____CrO42+______
(2)向滤液 1 中加入 BaCl2 ![]() 2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
①结合上述流程说明熟石灰的作用:_____。
②结合表中数据,说明选用Ba2 不选用Ca2处理废水的理由:_____。
③ 研究温度对CrO42 沉淀效率的影响。实验结果如下:在相同的时间间隔内,不同温度下CrO42- 的沉淀率(沉淀率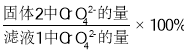 如图所示)
如图所示)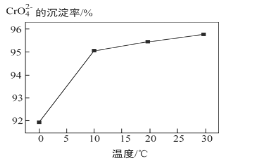
已知:![]()
CrO42- 的沉淀效率随温度变化的原因是_____。
(3)向固体2中加入硫酸,回收重铬酸。
①硫酸浓度对重铬酸的回收率如下图(左)所示。结合化学平衡移动原理,解释使用 0.450 mol/L 的硫酸时,重铬酸的回收率明显高于使用 0.225 mol/L 的硫酸的原因:_____。
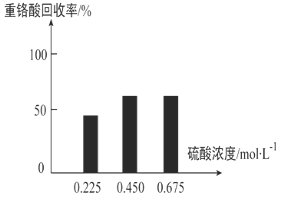
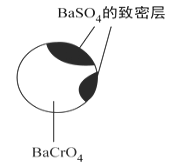
②回收重铬酸的原理如上图(右)所示。当硫酸浓度高于0.450 mol/L时,重铬酸的回收率没有明显变化,其原因是_____。
(4)综上所述,沉淀BaCrO4进一步回收重铬酸的效果与_____、_____、有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正确的是
A.淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B.纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C.油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D.蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
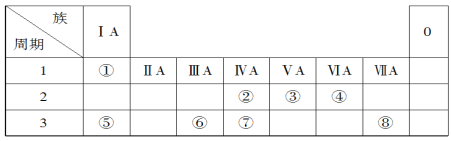
(1)地壳中含量居于第二位的元素在周期表中的位置是________________。
除稀有气体外,原子半径最大的元素是______,它的原子结构示意图是________。
(2)②的最高价氧化物的分子式为________;
⑦的最高价氧化物对应水化物的分子式为________;
最高价氧化物对应的水化物中酸性最强的是________。
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:________________________________。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是________。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林是常用的抗凝血药物。下面是利用 Michael 反应合成华法林的一种方法。
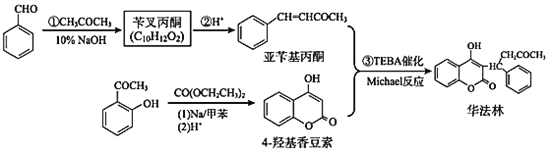
回答下列问题:
(1)![]() 的名称是_____。用银氨溶液检验其官能团的反应的化学方程式为________。
的名称是_____。用银氨溶液检验其官能团的反应的化学方程式为________。
(2)反应①~③中,属于加成反应的是_______(填序号)。
(3)苄叉丙酮的结构简式为 ______。
(4)![]() 中官能团的名称为_______、_______。
中官能团的名称为_______、_______。
(5)反应①除生成苄叉丙酮外,可能生成另一种化合物。该化合具有以下特征:
a.化学式为 C17H18O3;b.核磁共振氢谱有 6 组峰,且面积之比为 1:1:1:2:2:2;
则该化合物的结构简式为_________。
(6) 有多种同分异构体,属于芳香族化合物且为酯的同分异构体数目为 _______,其中不含“-CH3”的结构简式为 _______。
有多种同分异构体,属于芳香族化合物且为酯的同分异构体数目为 _______,其中不含“-CH3”的结构简式为 _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物.以芳香族化合物A为原料合成的路线如下:
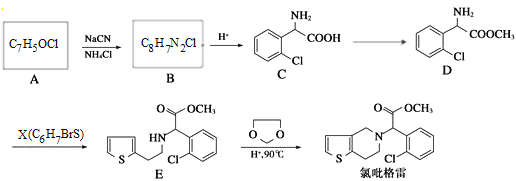
已知:①R-CHO![]() ,②R-CN
,②R-CN![]() RCOOH
RCOOH
(1)写出反应C→D的化学方程式______________,反应类型____________。
(2)写出结构简式.B____________,X____________。
(3)A属于芳香族化合物的同分异构体(含A)共有______种,写出其中与A不同类别的一种同分异构体的结构简式___________。
(4)两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,写出该反应的化学方程式________________。
(5)已知:![]() ,设计一条由乙烯、甲醇为有机原料制备化合物
,设计一条由乙烯、甲醇为有机原料制备化合物![]() 的合成路线流程图,无机试剂任选_____________。(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A
的合成路线流程图,无机试剂任选_____________。(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A![]() B…
B…![]() 目标产物)
目标产物)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com