
分析 (1)将少许混合物放入水中得到无色溶液和白色沉淀,一定不含有有色离子的物质,白色沉淀可能为碳酸钙或硫酸钡,所以无法确定一定存在的物质;
(2)根据焰色反应显示黄色可以判断一定存在硫酸钠,无法确定一定不存在的物质;
(3)取白色沉淀加入稀盐酸,沉淀完全溶解并放出气体,产生的气体为二氧化碳,说明一定含有碳酸钙,再根据沉淀完全溶解判断一定不存在硝酸钡;
根据以上分析,仍然无法确定是否含有硫酸铝.
解答 解:(l)得到的溶液为无色,所以一定不存在硫酸铜,因含有Cu2+的溶液是蓝色溶液,生成的白色沉淀可能为硫酸钡或碳酸镁,故答案为:CuSO4;溶液无色,而CuSO4溶液为蓝色;
(2)取溶液进行焰色反应,火焰呈黄色,证明溶液中存在钠离子,原混合物中一定含有硫酸钠;
(3)加入稀盐酸,沉淀完全溶解并放出气体,各物质中只有碳酸钙与盐酸反应生成气体,所以一定含有碳酸钙;由于沉淀完全溶解,而硫酸钡都不溶于盐酸,所以一定不含有硝酸钡,
根据以上分析,仍无法确定的物质是硫酸铝,肯定存在的物质是碳酸钙和硫酸钠,肯定不存在的物质是硫酸铜和硝酸钡,
故答案为:Al2(SO4)3; CaCO3、Na2SO4;Ba(NO3)2、CuSO4.
点评 本题考查了未知物的检验与鉴别,题目难度中等,注意掌握检验未知物的方法,能够根据反应现象判断未知物的组成,进行物质的检验时,要依据物质的特殊性质和特征反应进行分析,得出合理结论.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
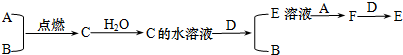
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮气化学性质不活泼,可用作食品防腐剂 | |
| B. | 硅胶无毒、无味、无腐蚀性,可用作食品干燥剂 | |
| C. | SiO2、Al2O3、MgO都有很高的熔点,可以制耐火材料 | |
| D. | 二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
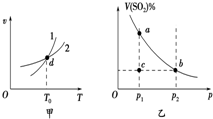
| A. | 图甲中,曲线1表示正反应速率和温度的关系,曲线2表示逆反应速率与温度的关系 | |
| B. | 图乙中,温度恒定时,a、b两点对应的反应速率:va>vb | |
| C. | 图甲中,d点表示温度为T0时,反应已经达到平衡 | |
| D. | 图乙中,温度恒定时,c点的反应正在向正反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
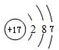 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加热 | B. | 加入催化剂 | C. | 减小压强 | D. | 增加C的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
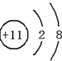 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com