
【题目】甲、乙、丙是三种常见的单质,A、B、C是三种常见的二元无机化合物,它们之间的转化关系如右图所示。请回答下列有关问题:
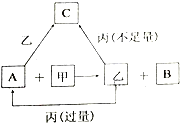
(1)若甲为常见气态非金属单质,丙为金属单质,三种单质中只有甲由短周期元素组成;甲与乙同主族、乙与丙同周期;它们的转化关系均在溶液中进行。则:
①甲物质的名称为___________。
②丙元素在元素周期表中的位置是___________。
③反应A+甲→乙+B的离子方程式为______________________。
④请简述B中阳离子的检验方法__________________________________。
(2)若甲为常见金属单质,乙为常见固态非金属单质,且所有物质组成元素均为短周期元素。则:
①乙的化学式为___________。
②A的电子式为___________。
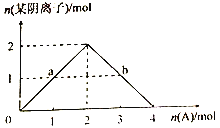
③将A缓慢通入氢氧化钠溶液中,所得溶液中的某种阴离子的物质的量随n(A)的通入转化关系如右图所示。图中a、b两点的溶液中水的电离程度的大小关系为a_______b(填“>”、“=”或“<")。若溶液X为图中曲线上任意一点,则向溶液X中逐滴加入盐酸至反应完全,消耗盐酸的物质的量最大为___________。
【答案】 氯气 第四周期第Ⅷ族 2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- 用试管取少量B溶液,然后向其中滴入几滴KSCN溶液,若溶液呈现血红色,证明有Fe3+存在 C ![]() < 4mol
< 4mol
【解析】根据题给信息,A+甲→乙+B 该反应为置换反应,若甲为常见气态非金属单质,三种单质中只有甲由短周期元素组成,甲与乙同主族;根据周期表中主族元素的置换规律:氯气置换溴,所以甲为氯,乙为溴,乙与丙同周期,丙为铁,A为溴化亚铁,B为氯化铁,溴与过量的铁生成溴化亚铁,溴与少量的铁生成溴化铁;
①正确答案:氯气;
② 铁元素在周期表中第四周期,第Ⅷ族;正确答案:第四周期、第Ⅷ族;
③ 溴化亚铁被氯气全部氧化为单质溴和氯化铁,该反应为置换反应;正确答案:
2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-;
④Fe3+的最简的检验方法滴加KSCN溶液,若溶液变为血红色,溶液中含有Fe3+;正确答案:用试管取少量B溶液,然后向其中滴入几滴KSCN溶液,若溶液呈现血红色,证明有Fe3+存在;
(2)甲为常见金属单质,乙为常见固态非金属单质,且所有物质组成元素均为短周期元素;
A+甲→乙+B 该反应为置换反应,金属置换非金属反应,金属镁在二氧化碳气体中燃烧,生成碳单质和氧化镁;A为二氧化碳,甲为镁,乙为碳,B为氧化镁;碳与足量的氧气燃烧变为二氧化碳,氧气不足,生成一氧化碳;
① 正确答案:C;
② 正确答案:![]()
③将二氧化碳缓慢通入氢氧化钠溶液中,当达到a点时,生成部分碳酸钠,所得混合液为氢氧化钠和碳酸钠;当二氧化碳继续通入,氢氧化钠完全反应,正好生成碳酸钠溶液,曲线达到最高点;继续通入二氧化碳,碳酸钠继续与二氧化碳反应,达到b 点,溶液变为碳酸钠和碳酸氢钠的混合液,直到最后,碳酸钠全部变为碳酸氢钠溶液; a点为氢氧化钠和碳酸钠混合液,溶液为强碱,抑制水的电离;b 点碳酸钠和碳酸氢钠的混合液,两种盐都能够促进水的电离,a<b; 正确答案:< ;从图像上看,当反应进行到最大值时,,阴离子的总量为2mol,恰好生成碳酸钠溶液,n(Na+)=4 mol, 向溶液X中逐滴加入盐酸至反应完全,,所得溶液的溶质为氯化钠,根据守恒原则,n(Cl-)=n(HCl)=4 mol,正确答案:4 mol;
.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现。铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图。下列说法正确的是( )

A. 铁片发生还原反应而被腐蚀
B. 铁片腐蚀最严重区域应该是生锈最多的区域
C. 铁片腐蚀中负极发生的电极反应:2H2O+O2+4e-===4OH-
D. 铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如下图所示装置来制备乙炔,并验证乙炔的某些化学性质,制备的 乙炔气体中往往含有少量的 H2S 气体,请按下列要求填空:
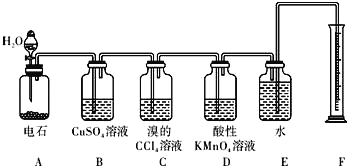
(1)实验室制乙炔的化学方程式是:_________________;为了得到较为平稳的乙炔气流, 装置 A 的分液漏斗中常用_____来代替水.
(2)装置 B 中CuSO4溶液的作用是_____.
(3)装置 D 中观察到的现象是_____
(4)若称取m g 电石,反应完全后,测得B处溴的CCl4溶液增重n g,则CaC2的纯度为_____(用m与n表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子能在强碱性溶液中大量共存,且溶液为无色透明的是( )
A.K+、MnO4-、Mg2+、Cl-B.Na+、Ba2+、HCO3-、NO3-
C.Na+、NO3-、CO32-、Cl-D.K+、H+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。
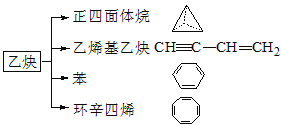
完成下列各题:
(1)乙炔在一定条件下制取苯的化学反应方程式是_________________________。
(2)正四面体烷的分子式为___________,其二氯取代产物有__________种。
(3)关于乙烯基乙炔分子的说法正确的是__________。
A.由乙炔通过取代反应制得
B.能使酸性KMnO4溶液褪色
C.1 mol乙烯基乙炔能与3 mol Br2发生加成反应
D.等物质的量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同
(4)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式有_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中应注重食谱营养搭配的均衡性,下列午餐食谱中最有利于学生身体发育的是
A. 馒头、榨菜、黄瓜、香蕉
B. 面条、醋溜土豆丝、素炒白菜
C. 米饭、糖醋排骨、粉蒸肉、清蒸鲈鱼
D. 米饭、红烧鲫鱼、西红柿蛋汤、蒜蓉生菜、苹果
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com