
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。
请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为 ,第一电离能最小的元素是 (填元素符号)。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是 (填化学式),呈现如此递变规律的原因是 。
 (3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为 、另一种的晶胞如图二所示,该晶胞的空间利用率为 ,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为 、另一种的晶胞如图二所示,该晶胞的空间利用率为 ,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为  (保留两位有效数字)。(
(保留两位有效数字)。( )
)
(4)D元素形成的单质,其晶体的堆积模型为 ,D的醋酸盐晶体局部结构如图
三,该晶体中含有的化学键是 (填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)向D的硫酸盐溶液中滴加过量氨水,观察到的现象是 。请写出上述过程的离子方程式: 。
【知识点】原子核外电子排布、晶胞计算、化学键
【答案解析】
(1)
| ↑↓ | ↑↓ | ↑↓ | ↑ |
3s 3p
(2)HF>HI>HBr>HCl (1分) HF分子之间形成氢键使其熔沸点较高,HI、HBr、HCl分子之间只有范德华力,相对分子量越大,范德华力越大(2分)
(3)sp2(1分) 34%(2分)
(4)面心立方最密堆积(1分) ①②③(1分)
(5)首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液(1分)
Cu2++2NH3·H2O===Cu(OH)2↓+2NH、Cu(OH)2+4NH3===[Cu(NH3)]2++2OH-(各1分,共2分)
解析:由题意得A为氢元素,B为碳元素,C为氯元素,D为29号元素是铜元素。
电负性最大的是氯元素,M层有7个电子其基态原子的价电子排布图为
| ↑↓ | ↑↓ | ↑↓ | ↑ |
第一电离能最小的是铜元素,填Cu
3s 3p
卤族元素的氢化物沸点由高到低的顺序是HF>HI>HBr>HCl ,HF分子之间形成氢键使其熔沸点较高,HI、HBr、HCl分子之间只有范德华力,相对分子量越大,范德华力越大,熔沸点较高。
图一中每个碳原子形成3个ρ键,形成3个杂化轨道,所以是sp2杂化。图二为金刚石晶胞中有8个原子,顶点一个、面心三个、晶胞内四个。这样可算原子体积。而晶胞中只有体对角线上的原子是密置的,体对角线与晶胞边长a的关系是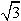 a =8r,算出来的空间利用率是34.0%。
a =8r,算出来的空间利用率是34.0%。
铜晶胞为面心立方最密堆积,图三醋酸铜晶胞中碳氧键、碳氢键为极性键,碳碳键为非极性键,铜氧间是配位键。选 ①②③。
(5)首先形成Cu(OH)2蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。化学反应为:Cu2++2NH3·H2O===Cu(OH)2↓+2NH、Cu(OH)2+4NH3===[Cu(NH3)]2++2OH-
【思路点拨】本题考查原子核外电子排布、晶胞计算、化学键,注意结构的计算,难度中等。


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
下列各组中两个反应所属反应类型相同的是( )
A.甲烷和氯气在光照下反应;乙烯能使溴水褪色
B.乙烷在氧气中燃烧;由乙烯制取聚乙烯
C.乙烯能使溴水褪色;乙烯能使酸性高锰酸钾溶液褪色
D.乙烯和水反应制乙醇;乙烯能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学学习、研究中,类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中正确的是
A. CO2和Na2 O2反应生成Na2CO3,推测:SO2和Na2O2反应生成Na2SO3
O2反应生成Na2CO3,推测:SO2和Na2O2反应生成Na2SO3
B.金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭
C. Fe3O4可表示为FeO·Fe2O3,推测:Pb3O4也可表示为PbO·Pb2O3
D. F、C l、 Br,、I的单质熔点依次升高,推测:N、 P、As、 Sb、Bi单质熔点也依次升高
l、 Br,、I的单质熔点依次升高,推测:N、 P、As、 Sb、Bi单质熔点也依次升高
查看答案和解析>>
科目:高中化学 来源: 题型:
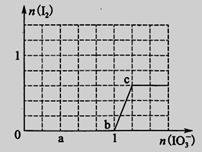
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题:
(1)写出a点反应的离子方程式________________;反应中还原剂是______________;被还原的元素是__。
(2)写出b点到c点反应的离子方程式_____________________________。
(3)若往100 mL 1 mol·L-1的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )
 A、若
A、若 为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
B、若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
C、若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
D、若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+B(g) 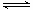 C(g)+D(g)过程中的能量变化如图所示,
C(g)+D(g)过程中的能量变化如图所示,
①正反应为放热反应,
②反应物总能量低于生成物总能量,
③反应物的总键能小于生成物的总键能,
④1molA与1molB充分反应后,能量变化为ΔE,
⑤加入催化剂后,反应加快,ΔE减小,
⑥反应达到平衡时,升高温度,A的转化率增大,
⑦升高温度可增大正反应速率,降低逆反应速率,
⑧E2是反应C(g)+D(g) 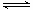 A(g)+B(g) 的活化能,
A(g)+B(g) 的活化能,
以上有关说法正确的是
A.⑤⑥⑦⑧ B.①②③④ C.①③⑤⑦ D.②⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中发生反应N2+3H2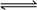 2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
回答下列问题:
(1)处于平衡状态的时间段是__________(填选项)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项),t1时刻________; t4时刻________。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________(填选项)。
A.t0~t1 B.t2~t3 C. t3~t4 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3 mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为( )
A.v (O2)= 0.0l mol·L-1·s-1 B.v (NO)=0.001 mol·L-1·s-1
C. v (NH3)=0.001 mol·L-1·s-1 D. v (H2O)=0.003 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com