
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:不详 题型:填空题
| | | a | |||||
| | | | | b | c | | |
| d | | e | | | | f | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.XO4- | B.XO32- | C.XO42- | D.XO43- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
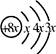 ;a与b形成化合物的电子式为:
;a与b形成化合物的电子式为: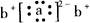 。下列叙述正确的是
。下列叙述正确的是| A.原子半径:a>c>d | B.非金属性:c>a>d |
| C.相应氢化物的沸点:d>c>a | D.c与a、c与b均能形成两种常见化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.它是一种共价化合物 |
| B.在加热时此化合物可以分解为PH3和HI或H2和I2 |
| C.这种化合物能跟碱反应 |
| D.该化合物可以由PH3和HI化合而成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
| B.NH3分子的空间构型是三角锥形;则BF3分子的空间构型也是三角锥形 |
| C.CO2和SiO2化学式相似,则CO2与SiO2的物理性质也相似 |
| D.第二周期元素氢化物稳定性顺序是HF >H2O >NH3;则第三周期元素氢化物稳定性顺序 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com