
【题目】下列有关仪器使用方法或实验操作正确的是![]()
A.洗净的锥形瓶和容量瓶可以放进烘箱烘干
B.酸式滴定管装标准溶液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
科目:高中化学 来源: 题型:
【题目】常温下,已知水的电离方程式是H2O![]() H++OH-,下列叙述正确的是( )
H++OH-,下列叙述正确的是( )
A.水的电离程度只受温度的影响
B.向水中加入少量盐酸,c(H+)增大,Kw不变
C.粒子![]() 对水的电离平衡不会产生影响
对水的电离平衡不会产生影响
D.向水中加入少量固体NH4Cl,平衡向逆反应方向移动,pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.NaClO溶液中通入少量CO2,ClO﹣水解程度增大,溶液碱性增强
B.铁片镀锌时,铁片与外电源的正极相连
C.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则ΔH<0
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)![]() NO(g)+SO3(g),通入少量O2,
NO(g)+SO3(g),通入少量O2,![]() 的值及SO2转化率不变
的值及SO2转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下将1mol N2和2molH2的混合气体通入1L密闭容器中,在一定条件下发生反应,达到化学平衡时,测得混合气体中N2的物质的量为0.5mol。求:
(1)平衡时H2的转化率_______________。
(2)此温度下反应N2 (g) + 3H2(g)![]() 2NH3 (g)的平衡常数_______________。
2NH3 (g)的平衡常数_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1molL-1的醋酸溶液和氨水溶液各20mL,分别用0.1molL-1NaOH溶液、0.1molL-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是
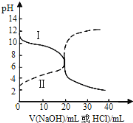
A.曲线Ⅰ:滴加溶液到10mL时![]()
B.曲线Ⅱ:滴加溶液到20mL时:![]()
C.根据滴定曲线,可得![]()
D.由曲线Ⅱ可知,选用酚酞和选用甲基橙作指示剂,消耗NaOH溶液的体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某血液样品中钙离子的含量,可取该样品2.00mL用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用1.000×10-4molL-1酸性KMnO4标准溶液滴定,到达终点时用去20.00mL标准液。则下列说法中错误的是( )
A.用酸性KMnO4(aq)滴定H2C2O4(aq)的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
B.KMnO4标准溶液应用碱式滴定管盛装
C.滴定终点时的现象为:最后1滴标准KMnO4(aq)使锥形瓶中溶液由无色变为浅紫色,且约半分钟内不褪色
D.经计算该样品中钙离子浓度为1.000×10-4gmL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数为82.0%,为了验证其纯度,用浓度为0.2molL-1的盐酸进行滴定,结果偏高,试分析可能由下列哪些实验操作引起的( )
A.转移待测液至容量瓶时,未洗涤烧杯
B.滴定到终点时,滴定管尖嘴悬有液滴
C.滴定时,反应容器摇动太激烈,有少量液体溅出
D.读酸式滴定管开始时仰视,读终点时俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和 I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g),1 mol H2 完全反应放出 akJ热量。已知:(a、b、c 均大于零)。下列说法不正确的是
2HI(g),1 mol H2 完全反应放出 akJ热量。已知:(a、b、c 均大于零)。下列说法不正确的是
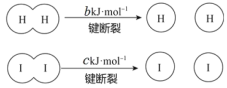
A.反应物的总能量高于生成物的总能量
B.断开 1 mol H—H 键和 1 mol I—I 键所需能量大于断开 2 mol H—I 键所需能量
C.断开 2 mol H—I 键所需能量约为(c+b+a)kJ
D.向密闭容器中加入 2 mol H2 和 2 mo l I2,充分反应放出的热量小于 2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发)。下列说法正确的是( )
时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发)。下列说法正确的是( )

A.点a所示溶液中:![]()
B.点b所示溶液中:![]()
C.点c所示溶液中:![]()
D.点d所示溶液中:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com