
【题目】下列排列顺序正确的是( )
①热稳定性:![]() ②原子半径:
②原子半径:![]() ③酸性:
③酸性:![]() ④得电子能力:
④得电子能力:![]()
A.①③B.②④C.①④D.②③
【答案】B
【解析】
①O、F属于同周期元素,从左至右,非金属性增强,则非金属性F>O,O、S属于同主族元素,从上往下,非金属性减弱,则非金属性O>S,所以非金属性F>O>S,非金属越强,气态氢化物越稳定,则气态氢化物的热稳定性为HF>H2O>H2S,故①错误;
②电子层数越多半径越大,Na、Mg电子层三层,O电子层二层,则O原子半径最小,电子层数相同的,原子序数大的原子半径小,Na、Mg电子层数相同,原子序数Na<Mg,原子半径Na>Mg,则原子半径:Na>Mg>O,故②正确;
③P、S、Cl属于同周期元素,从左至右,非金属性增强,则非金属性P<S<Cl,非金属性越强,其最高价氧化物的水化物的酸性越强,则酸性:H3PO4<H2SO4<HClO4,故③错误;
④Be、Mg、Ca属于同主族元素,从上往下,金属性增强,则金属性Be<Mg<Ca,金属性越强,变为离子后,得电子能力越弱,则得电子能力:Be2+>Mg2+>Ca2+,故④正确;由上分析可知②④正确;
答案为B。


科目:高中化学 来源: 题型:
【题目】化学兴趣小组同学想用金属钠和空气制备纯度较高的Na2O2(N2不与金属钠应),可利用的装置如下。回答下列问题:
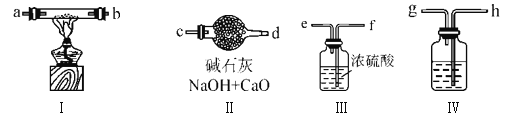
(1)装置Ⅳ中盛放的药品是________,若没有该装置可能导致生成的Na2O2中含有碳酸钠,其反应方程式为____________________________。
(2)若规定气体的气流方向从左到右,各仪器接口的标号字母(a、b……)顺序:
空气进入h,________接________,________接________,________接________,d
(3)装置Ⅱ的作用是_____________________________________________________。
(4)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞溶液变红是因为________________,红色褪去的可能原因是____________________。
② 加入MnO2反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国对雾霾的治理重视有加。研究NO2、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)利用钠碱循环法可脱除烟气中的SO2。在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,发生反应的离子方程式是__________________。
(2)在恒温恒容的容器中充入3molCO,3molH2发生反应2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g),下列说法可以判断反应一定达到平衡状态的是____________。
CH3OCH3(g)+H2O(g),下列说法可以判断反应一定达到平衡状态的是____________。
A.CO和CH3OCH3(g)的生成速率相等
B.混合物中CO的体积分数保持不变
C.反应容器中的压强不再变化
D.反应容器内CO、H2、CH3OCH3(g)、H2O(g)四者共存
E.反应容器中混合气体的平均摩尔质量保持不变
(3)利用反应6NO2+8NH3=7N2+12H2O设计为电池可消除NO2,其简易装置如图所示。
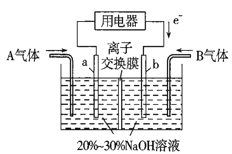
①b极的电极反应式为______________________。
②常温下,若用该电池电解0.6L饱和KCl溶液,一段时间后,测得饱和KCl溶液pH变为13,则理论上a极上消耗A气体的体积为_____mL(气体处于标准状况;假设电解过程中溶液体积不变)。
(4)化学上采用NH3处理NxOy不仅可以消除污染,还可作为工业生产的能量来源。
已知:①2NO(g)=N2(g)+O2(g) H1= -177kJ.mol-1
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) H2= -1253.4kJ.mol-1
则用NH3处理NO生成氮气和气态水的热化学方程式为___________________。
(5)氨氧化物可用碱溶液吸收。若NO和NO2混合气体被NaOH溶液完全吸收,只生成一种盐,则该反应的化学方程式为____________。已知常温下.Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq)![]() NaNO2(aq)+H2O(1)的平衡常数为________。
NaNO2(aq)+H2O(1)的平衡常数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】头孢拉定又名先锋霉素,是常用的一种抗生素,其结构简式如下:
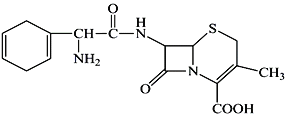
下列说法不正确的是 ( )
A. 头孢拉定的分子式是C16H19N3O4S,分子中有多种官能团
B. 头孢拉定与Na2CO3溶液、NaHCO3溶液都可以反应
C. 头孢拉定既可与盐酸反应,也可与NaOH溶液反应
D. 1mol头孢拉定最多可与5mol H2和3mol Br2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列有关实验的叙述,错误的是(填序号)_______;
A 用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B 分馏石油时,温度计的末端必须插入液面下
C 用分液漏斗分离环己烷和水的混合液体
D 用浓氨水洗涤做过银镜反应的试管
E 配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止
(2)人造羊毛在许多方面比天然羊毛更优良,其分子存在如下结构:
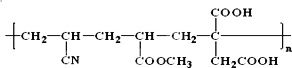
合成它的单体有_________。
(3)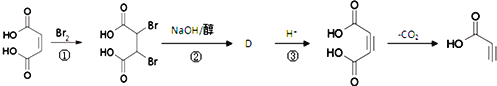
写出反应②的化学方程式 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于加成反应的是( )
A. CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
B. CH2===CH2+HCl―→CH3CH2Cl
C. CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O
D. 2CH3CH3+7O2![]() 4CO2+6H2O
4CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1)M元素是________(填元素符号)。
(2)Z、W形成的气态氢化物的稳定性为________>________。(填化学式)
(3)写出M2Z2的电子式:________,写出M2Z2与水反应的离子方程式: _____________。
(4)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与铜反应,离子方程式为______。
(5)由X、Y、Z、W四种元素组成一种离子化合物A,已知:①1 mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是________(填化学式)。写出气体B与氯水反应的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。放电时总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
①写出放电时负极的电极反应式:__。
②铅蓄电池放电时,溶液的pH将_(填增大、减小或不变);当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为__。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为___;若将负极材料改为CH4,写出其负极反应方程式__。

(3)法国格勒诺布尔(Grenoble)约瑟夫﹒傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶(蛋白质)的作用下发生反应:C6H12O6+6O2![]() 6CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
6CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
A.该生物燃料电池不能在高温下工作
B.该电池负极的电极反应式为:C6H12O6+6H2O-24e-=6CO2↑+24H+
C.消耗1mol氧气时转移4mol电子,H+向负极移动
D.提高葡萄糖生物燃料电池的效率,可使其在将来为更多可植入医疗设备提供电能
(4)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂—碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中___作正极,负极的电极反应为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com