


 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +2NaBr.
+2NaBr.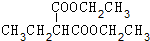 +(CH3)2CHCH2CH2Br+CH3CH2ONa→
+(CH3)2CHCH2CH2Br+CH3CH2ONa→ +CH3CH2OH+NaBr.
+CH3CH2OH+NaBr. .
. .
. 分析  在氢氧化钠水溶液、加热条件下发生水解反应生成A为
在氢氧化钠水溶液、加热条件下发生水解反应生成A为 ,对比A、B分子式可知,A中羟基被氧化为醛基,则B为
,对比A、B分子式可知,A中羟基被氧化为醛基,则B为 ,B进一步氧化生成C为
,B进一步氧化生成C为 ,C与乙醇发生酯化反应生成D,结合题目信息及F的结构简式,可知D为
,C与乙醇发生酯化反应生成D,结合题目信息及F的结构简式,可知D为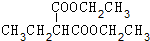 ,E为
,E为 ,试剂Ⅱ为
,试剂Ⅱ为 ,以此来解答.
,以此来解答.
解答 解:(1)试剂Ⅰ为CH3CH2OH,化学名称是:乙醇,化合物B为 ,含有的官能团名称是:醛基,第④步的化学反应类型是:酯化反应或取代反应,
,含有的官能团名称是:醛基,第④步的化学反应类型是:酯化反应或取代反应,
故答案为:乙醇;醛基;酯化反应或取代反应;
(2)第①步反应的化学方程式为 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +2NaBr,
+2NaBr,
故答案为: +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +2NaBr;
+2NaBr;
(3)第⑤步反应的化学方程式为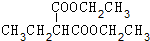 +(CH3)2CHCH2CH2Br+CH3CH2ONa→
+(CH3)2CHCH2CH2Br+CH3CH2ONa→ +CH3CH2OH+NaBr,
+CH3CH2OH+NaBr,
故答案为: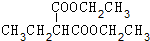 +(CH3)2CHCH2CH2Br+CH3CH2ONa→
+(CH3)2CHCH2CH2Br+CH3CH2ONa→ +CH3CH2OH+NaBr;
+CH3CH2OH+NaBr;
(4)试剂Ⅱ相对分子质量为60,由上述分析可知,其结构简式是 ,故答案为:
,故答案为: ;
;
(5)化合物B( )的一种同分异构体G与NaOH溶液共热反应,生成乙醇和化合物H,H可发生聚合反应,则H的结构简式为CH2=CHCOONa,H在一定条件下发生聚合反应得到高吸水性树脂,该聚合物的结构简式是
)的一种同分异构体G与NaOH溶液共热反应,生成乙醇和化合物H,H可发生聚合反应,则H的结构简式为CH2=CHCOONa,H在一定条件下发生聚合反应得到高吸水性树脂,该聚合物的结构简式是 ,
,
故答案为: .
.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团变化、碳原子数变化、有机反应条件及有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | CCl4+H2$→_{△}^{催化剂}$ CHCl3+HCl | B. | 2CH2=CH2+O2$→_{△}^{催化剂}$2CH3CHO | ||
| C. |  +HNO3$→_{50℃-60℃}^{浓H_{2}SO_{4}}$+H2O+ +HNO3$→_{50℃-60℃}^{浓H_{2}SO_{4}}$+H2O+ | D. |  +3H2$→_{△}^{Ni}$ +3H2$→_{△}^{Ni}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为35的氯原子:35Cl | B. | 氟原子的结构示意图: | ||
| C. | 氯化铵的电子式: | D. | 明矾的化学式:Al2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q为最简整数比).A、B、C、D的物质的量变化如图所示.
T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q为最简整数比).A、B、C、D的物质的量变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1 KSCN溶液,静置 | 出现白色沉淀 |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1 Fe(NO3)3溶液 | 溶液变红色 |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1 AgNO3溶液 | 现象a出现白色沉淀,溶液红色变浅 |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1 KI溶液 | 出现黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴极上产生红色物质 | B. | 阴极附近溶液呈红色 | ||
| C. | 阴极上产生氯气 | D. | 阳极上产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X气体可以是N2,目的是做保护气,抑制CuCl2•2H2O加热过程可能的水解 | |
| B. | CuCl与稀硫酸反应的离子方程式为:2Cu++4H++SO42-═2Cu2++SO2↑+2H2O | |
| C. | 途径1中产生的Cl2可以回收循环利用,也可以通入饱和CaCl2溶液中除去 | |
| D. | 途径2中200℃下反应的化学方程式为:Cu2(OH)2Cl2$\frac{\underline{\;加热\;}}{\;}$2CuO+2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 第一组 | 第二组 | 第三组 | 第四组 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com