
【题目】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。提示:图中A代表沉淀或者溶液

(1)检验提纯后的KCl中是否还含有SO42-的方法是____________________________。
(2)用提纯后的KCl配制980 mL 1.00 mol/L的氯化钾溶液,回答下列问题:
①根据计算,所需称量的KCl的质量为__________。
②容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线这五项中的______。(填数字符号)
③下列操作会使所配溶液浓度偏低的是__________(填选项代号)。
A.配制前容量瓶内壁刻度线以下存有水珠 B.没有洗涤烧杯内壁
C.转移溶液时部分溶液溅出容量瓶外 D.定容时俯视
(3)试剂Ⅰ的名称为______,试剂Ⅱ的化学式为______,试剂Ⅲ的化学式为_____。
【答案】取少量KCl晶体溶于水中,再加入适量稀HCl后,加入适量BaCl2,若有白色沉淀生成,则证明含有SO42-,反之则没有 74.5g ①、③、⑤ BC 氯化钡 K2CO3 HCl
【解析】
据氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质,除去碳酸根离子和硫酸根离子,需要加入过量的氯化钡溶液,然后过滤后得到氯化钡、氯化钾的混合溶液A,然后加入过量的碳酸钾溶液,除去氯化钡,过滤得到氯化钾和碳酸钾的混合溶液,再加入过量的盐酸,除去碳酸钾,最后经过加热浓缩,蒸发结晶,除去多余的稀盐酸,得到氯化钾晶体,据此进行分析回答有关的问题。
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质,除去碳酸根离子和硫酸根离子,需要加入过量的氯化钡溶液,然后过滤后得到氯化钡、氯化钾的混合溶液A,然后加入过量的碳酸钾溶液,除去氯化钡,过滤得到氯化钾和碳酸钾的混合溶液,再加入过量的盐酸,除去碳酸钾,最后经过加热浓缩,蒸发结晶,除去多余的稀盐酸,得到氯化钾晶体;
(1)检验提纯后的KCl中是否还含有SO42-的方法是取少量KCl晶体溶于水中,再加入适量稀HCl后,加入适量BaCl2,若有白色沉淀生成,则证明含有SO42-,反之则没有;
(2)用提纯后的KCl配制980 mL 1.00 mol/L的氯化钾溶液,则
①实验室无980mL容量瓶,则选择1000mL容量瓶,即配制1000 mL 1.00 mol/L的氯化钾溶液,所需称量的KCl的质量为1L×1.00 mol/L×74.5g/mol=74.5g;
②容量瓶是定容容器,标有温度、容量及刻度线,不标浓度和压强,即选①、③、⑤;
③A.配制前容量瓶内壁刻度线以下存有水珠,不影响溶质和溶液的体积,即对所配溶液浓度无影响,故A错误;
B.没有洗涤烧杯内壁,容量瓶内溶质减少,则所配溶液浓度偏低,故B正确;
C.转移溶液时部分溶液溅出容量瓶外,容量瓶内溶质减少,则所配溶液浓度偏低,故C正确;
D.定容时俯视,溶液的体积偏小,则所配溶液浓度偏高,故D错误;
故答案为BC;
(3)据以上分析可知:试剂Ⅰ的名称为氯化钡,试剂Ⅱ的化学式为K2CO3,试剂Ⅲ的化学式为HCl。


科目:高中化学 来源: 题型:
【题目】有机物R是金银花的一种成分,具有广谱抗病毒功效,键线式为 (已知CH2=CHCH2OH的键线式为
(已知CH2=CHCH2OH的键线式为![]() )。下列说法错误的是( )
)。下列说法错误的是( )
A.R能发生加成、氧化、取代反应
B.用酸性高锰酸钾溶液可以确认R含碳碳双键
C.R分子中所有碳原子可能共平面
D.![]() CHO与R互为同分异构体
CHO与R互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列叙述中,正确的是( )
A.氧气的摩尔质量是32
B.2molNaCl固体溶解于1L水所得溶液的物质的量浓度为2mol/L
C.标准状况下同体积的O2和O3中所含分子数相等
D.在标准状况下,体积为22.4L的物质都是1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氮氧化物是形成光化学烟雾和酸雨的一个重要原因,用CH4催化还原NOx可在一定程度上消除氮氧化物的污染。
已知:![]() △H=-1160kJ·mol-1
△H=-1160kJ·mol-1
![]() △H=+293kJ·mol-1
△H=+293kJ·mol-1
则该条件下,CH4催化还原NO2消除污染的热化学方程式为________________________。
(2)乙炔(CH≡CH)是重要的化工原料。工业上可用甲烷裂解法制取乙炔:![]() 同时发生副反应:
同时发生副反应:![]() ;甲烷裂解时,几种气体平衡时分压(Pa)的对数即lgP与温度(℃)之间的关系如图所示。根据图判断,反应
;甲烷裂解时,几种气体平衡时分压(Pa)的对数即lgP与温度(℃)之间的关系如图所示。根据图判断,反应![]() △H___0(填“>”或“<”)。
△H___0(填“>”或“<”)。

1725℃时,向恒容密闭容器中充入CH4,达到平衡时CH4生成C2H2的平衡转化率为_____。该温度下,![]() 的平衡常数Kp=_______[注:用平衡分压(Pa)代替平衡浓度(mol·L-1)进行计算]。
的平衡常数Kp=_______[注:用平衡分压(Pa)代替平衡浓度(mol·L-1)进行计算]。

(3)利用在特定条件下用铂电极(阳极为铂丝)电解饱和硫酸氢钾溶液的方法制备K2S2O8(过二硫酸钾)。在低温下电解液中主要含有K+、H+和![]() 离子,电流通过溶液后发生反应。阳极区电极反应式为______________________________,X为_________交换膜(填“质子”、“阳离子”或“阴离子”),当电路中通过0.2mol e-时,两边溶液质量的变化差为_________。
离子,电流通过溶液后发生反应。阳极区电极反应式为______________________________,X为_________交换膜(填“质子”、“阳离子”或“阴离子”),当电路中通过0.2mol e-时,两边溶液质量的变化差为_________。
(4)甲烷燃料电池采用铂为电极,两电极上分别通入CH4和O2,电解质溶液为300mL 1.0mol·L-1的NaOH溶液。当O2通入量为8.96L(标准状况)且反应完全时,所得溶液中各离子浓度由大到小的顺序为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计了如下实验测定海带中碘元素的含量,依次经过以下四个步骤,下列图示装置和原理能达到实验目的的是( )
A. 灼烧海带:
B. 将海带灰溶解后分离出不溶性杂质: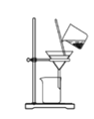
C. 制备Cl2,并将I-氧化为I2:
D. 以淀粉为指示剂,用Na2S2O3标准溶液滴定: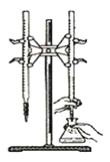
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅的单质、氧化物、盐在现代工业中有着重要用途。
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,盛有PbO2的圆底烧瓶中滴加浓盐酸,产生黄绿色气体,其反应的化学方程式为_______。
(2)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
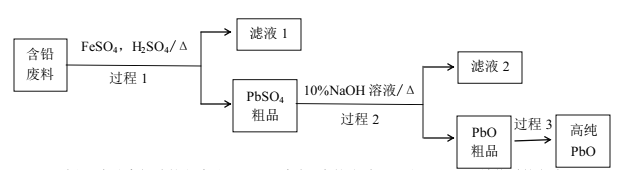
过程1中分离提纯的方法是___,滤液2中的溶质主要是____填物质的名称)。过程1中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是_______。
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
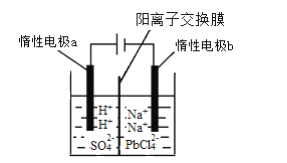
①写出电解时阴极的电极反应式_________。
②电解过程中通过阳离子交换膜的离子主要为____。
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向____极室(填“阴”或者“阳”)加入____(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO中Cl的化合价为__________,有较强的_________(填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_________。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为_____________________。
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为_________________。
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是__________。该图示的总反应为_______

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸式盐NaHY的水溶液c(OH-)>c(H+),下列叙述正确的是
A. H2Y的电离方程式:H2Y![]() 2H++Y2-
2H++Y2-
B. HY-的水解方程式:HY-+ H2O![]() H3O++ Y2-
H3O++ Y2-
C. 该酸式盐溶液中离子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H+)
D. 该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为1 L的恒容密闭容器中按不同方式投入反应物,发生反应CO(g)+2H2(g)![]() CH3OH(g)(正反应放热),测得反应的相关数据如下:
CH3OH(g)(正反应放热),测得反应的相关数据如下:
容器 | 容器1 | 容器2 | 容器3 |
反应温度T/K | 500 | 500 | 600 |
反应物投入量 | 1 mol CO、 2 mol H2 | 2 mol CH3OH | 1 mol CO、 2 mol H2 |
平衡v正(H2)/(mol·L-1·s-1) | v1 | v2 | v3 |
平衡c(CH3OH)/(mol·L-1) | c1 | c2 | c3 |
平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的转化率α | α1(CO) | α2(CH3OH) | α3(CO) |
平衡常数K | K1 | K2 | K3 |
下列叙述正确的是( )
A. v1<v2,2c1>c2B. α1(CO)>α3(CO),v1<v3
C. p2>2p3,K1<K3D. c2>2c3,α2(CH3OH)+α3(CO)<1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com