
| 40 |
| 7-2 |
 ,
, .
.

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
| A、2p轨道上只有一个空轨道的X原子与3p轨道上只有一个空轨道的Y原子 |
| B、原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C、原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| D、最外层都只有一个电子的X、Y原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
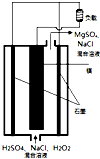 镁-过氧化氢燃料电池是具有比能量高、安全方便等优点,其总反应为Mg+H2O2+H2SO4=MgSO4+2H2O,结构示意图如图所示,关于该电池的叙述正确的是( )
镁-过氧化氢燃料电池是具有比能量高、安全方便等优点,其总反应为Mg+H2O2+H2SO4=MgSO4+2H2O,结构示意图如图所示,关于该电池的叙述正确的是( )| A、电池内部可以使用MnO2作填料 |
| B、电池工作时,H+向Mg电极移动 |
| C、电池充电时,Mg应与电源的负极相连 |
| D、电池工作时,正极周围溶液的pH将不断变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
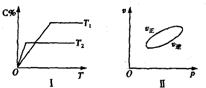 可逆反应aA(g)+bB(g)?cC(g)+dD(s)△H=QkJ/mol,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图I所示,反应速率(v)与压强(p)的关系如图II所示.据图分析,以下说法正确的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(s)△H=QkJ/mol,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图I所示,反应速率(v)与压强(p)的关系如图II所示.据图分析,以下说法正确的是( )| A、T1<T2,Q>0 |
| B、增大压强,物质B的转化率减小 |
| C、至反应达平衡时,混合气体的密度会变化 |
| D、a+b>c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、活化分子的总数越多,反应速率越快 |
| B、升高温度,活化分子百分数不变,活化分子数增多,化学反应速率增大 |
| C、使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大 |
| D、加入反应物,使活化分子百分数增大,化学反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2:3 |
| B、6:3:2 |
| C、1:1:1 |
| D、2:1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com