
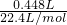 =0.02mol,根据电子转移守恒可知,参加反应的铜的物质的量为
=0.02mol,根据电子转移守恒可知,参加反应的铜的物质的量为 =0.03mol,根据铜元素守恒可知,溶液中n[Cu(NO3)2]=0.03mol,溶液中n(NO3-)=0.06mol.
=0.03mol,根据铜元素守恒可知,溶液中n[Cu(NO3)2]=0.03mol,溶液中n(NO3-)=0.06mol.

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013-2014学年黑龙江省佳木斯市高三第三次调研化学试卷(解析版) 题型:选择题
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体336mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
A.5.76 B.2.88 C.1.44 D.4.32
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省高三第四次模拟考试(理综)化学部分 题型:选择题
将一定质量的铜粉加入到100mL某浓度的稀硝酸中,充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器剩有铜粉m2g,则(m1-m2)为
A.5.76 B.2.88 C.1.92 D.0
查看答案和解析>>
科目:高中化学 来源:2010年河北省高三押题(理科综合)化学部分 题型:选择题
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
A.5.76 B.2.88 C.1.92 D.0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com