
| A.硫酸 | B.磷酸 | C.硝酸锌 | D.氯化铜 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
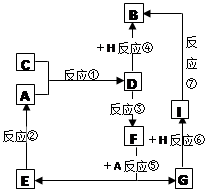
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3 : 2 | B.3 : 5 | C.4 : 3 | D.3 : 4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
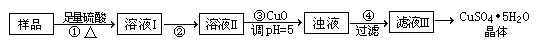
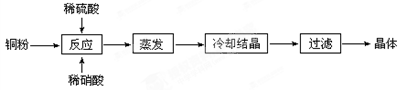
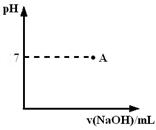
| A.醋酸 | B.草酸 | C.苯甲酸 | D.苯酚 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②④⑤ | C.①③⑥ | D.①②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝片表面的紫红色沉积物为Cu ,离子方程式为2Al+3Cu2+=3Cu+2Al3+ |
| B.生成的气体是H2,生成的蓝色沉淀为Cu(OH)2,产生该现象的离子方程式为3Cu2++6H2O+2Al=3Cu(OH)2↓+3H2↑+2Al3+ |
| C.一段时间后反应速率明显加快的原因一定是;反应放热,使溶液温度升高,反应速率加快 |
| D.溶液中出现的黑色物质可能是氧化铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
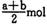 B (a — b) mol
B (a — b) mol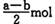 D. (a+b) mol
D. (a+b) mol查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com