
| A、8:3 |
| B、213:136 |
| C、34:213 |
| D、213:34 |
科目:高中化学 来源: 题型:
| A、反应物浓度等于生成物浓度 |
| B、容器中N2、H2、NH3浓度之比为1:3:2 |
| C、3v(N2正)=v(H2正) |
| D、反应混合体系的压强不随时间的变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧的摩尔质量是32g/mol |
| B、Al3+的摩尔质量是27g/mol |
| C、2molCO2的质量是88g/mol |
| D、1molH2S的摩尔质量是34g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AB |
| B、AB2 |
| C、AB3 |
| D、A2B3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子核外电子排布呈周期性变化 |
| B、元素的相对原子质量逐渐增大 |
| C、原子半径呈现从大到小的周期性变化 |
| D、元素化合价呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解质在溶液中存在电离平衡状态 |
| B、电离平衡状态时v结合=v电离=0 |
| C、弱电解质溶液中,既存在离子也存在分子 |
| D、电解质的电离是可逆过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | ||||
| B、Ba(OH)2溶液中逐滴滴加NaHSO4至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | ||||
C、用饱和氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O
| ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2 Fe(OH)3=2 FeO42-+3Cl-+5H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
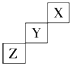 短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法中正确的是( )
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法中正确的是( )| A、Z可能是活泼金属元素 |
| B、X的最高价氧化物对应的水化物是一种强酸 |
| C、Y元素原子的最外层电子数为7 |
| D、Z的最高价氧化物对应水化物的化学式为HZO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试管编号 | 加3%Na2S2O3溶液/ml | 加H2O/ml | 加H2SO4(1:5)/滴 | 出现浑浊所用时间/s |
| ① | 3 | 3 | 5 | a |
| ② | 4 | 2 | 5 | b |
| ③ | 5 | 1 | 5 | c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com