
分析 A元素原子的最外层电子数是次外层电子数的2倍,应为C元素,B和C可形成BC4型化合物,则B为+4价,结合原子序数关系可知B为Si,则C为Cl,以此解答该题.
解答 解:A元素原子的最外层电子数是次外层电子数的2倍,应为C元素,B和C可形成BC4型化合物,则B为+4价,结合原子序数关系可知B为Si,则C为Cl,
(1)由以上分析可知A为C,B为Si,C为Cl,故答案为:C;Si;Cl;
(2)非金属性Cl>C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性最弱的是HClO4,故答案为:HClO4;
(3)B为Si,制备硅酸,可由二氧化硅与氢氧化钠溶液反应,然后再与盐酸反应,可生成硅酸,离子方程式为SiO2+2OH-=SiO32-+H2O、SiO32-+H+=H2SiO3↓,
故答案为:SiO2+2OH-=SiO32-+H2O;SiO32-+H+=H2SiO3↓.
点评 本题考查结构性质位置关系应用,为高考常见题型,题目侧重考查原子结构和元素的单质、化合物的性质,元素的推断是解答本题的关键,注意对元素周期律的理解.


科目:高中化学 来源: 题型:实验题
 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.263 | B. | 2.63 | C. | 0.132 | D. | 1.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①④ | B. | ①④⑥ | C. | ①④⑥⑦ | D. | ③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验中要配制490mL 0.2mol/L KCl溶液,需要托盘天平称量7.3g KCl固体 | |
| B. | 室温下,浓度均为0.1mol/L Na2S2O3和H2SO4溶液,分别取6mL与10mL混合、10mL与10mL混合,可验证Na2S2O3浓度对反应速率的影响 | |
| C. | 往盛有少量淀粉溶液的试管中加入一定量稀硫酸,加热3~4分钟后,再加入NaOH溶液至碱性,最后加入银氨溶液并水浴加热,有银镜产生 | |
| D. | 在中和热的测定实验中,将KOH溶液迅速倒入装有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH | B. | CH3OCOOCH3 | C. | CH3CH2C(CH3)3 | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
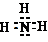 ;C气体的化学式是SO2.
;C气体的化学式是SO2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯的一氯取代物有三种同分异构体,它们的熔沸点各不相同 | |
| B. | CH2O2和C2H4O2分子组成上相差一个CH2,所以互为同系物 | |
| C. | 乙醛分别与O2,银氨溶液,新制氢氧化铜反应,均体现了乙醛的还原性 | |
| D. | 淀粉,纤维素,蛋白质都属于天然高分子化合物,可作为人体的供能物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com