
| A. | 4gNaOH固体所含电子总数为2NA | |
| B. | 22.4lL C2H6所含化学键总数为7 NA | |
| C. | 6g SiO2所含分子数为0.1NA,化学键总数为0.4 NA | |
| D. | 0.1 mol•L-1NH4Cl溶液中,NH${\;}_{4}^{+}$与Cl-数之和小于0.2NA |
分析 A、求出NaOH的物质的量,然后根据1molNaOH中含20mol电子来分析;
B、乙烷所处的状态不明确;
C、二氧化硅不是由分子构成的;
D、溶液体积不明确.
解答 解:A、4gNaOH的物质的量为n=$\frac{4g}{40g/mol}$=0.1mol,而1molNaOH中含20mol电子,故0.1mol钠含2mol电子即2NA个,故A正确;
B、乙烷所处的状态不明确,故乙烷的物质的量无法计算,故B错误;
C、二氧化硅是原子晶体,不是由分子构成的,故无二氧化硅分子,故C错误;
D、溶液体积不明确,故溶液中的铵根离子和氯离子之和无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 元素 | X | Y | Z | R | T |
| 原子半径/nm | 0.037 | 0.077 | 0.074 | 0.186 | 0.102 |
| 主要化合价 | +1 | +4、-4 | -2 | +1 | +6、-2 |
| A. | X、Y、Z 位于同一周期 | |
| B. | R 与 Z 所形成的化合物均只含离子键 | |
| C. | 氢化物的沸点:Y<Z<T | |
| D. | 第一电离能:Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
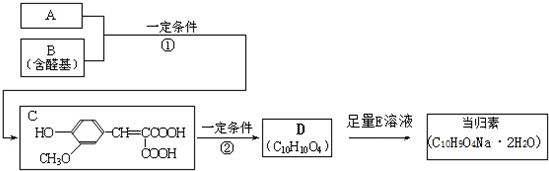
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 | |
| B. | 该元素的单质常温下不与浓硫酸反应 | |
| C. | 该元素的单质无需特别保存,因为其性质稳定,不易与空气成分反应 | |
| D. | 该元素的最高价氧化物对应的水化物只能与酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:3Ba2++3SO42-+2Al3++6OH-═2BaSO4↓+2Al(OH)3↓ | |
| B. | 醋酸除去水垢:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 碳酸氢钠和偏铝酸钠反应:HCO3-+AlO2-+H2O═CO32-+Al(OH)3↓ | |
| D. | 向硫酸铜中加入过量氨水:Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | Y是电源的正极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2ˉ,CO2+2e-═CO+O2- | |
| C. | 总反应可表示为:H2+CO2═H2+CO | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和Na2O2都属于盐 | B. | KOH和KHCO3都属于碱 | ||
| C. | H2SO4和H3PO4都属于酸 | D. | Na2O和Na2SiO3都属于氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2S和HCl | B. | Na2S和H2SO4 | C. | Na2SO3和HCl | D. | Na2SO3和H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的低价氧化物能使Z单质的水溶液褪色 | |
| B. | X的氢化物溶于水显酸性 | |
| C. | 其离子半径大小:Z>Y>X | |
| D. | X的氢化物和Z的最高价氧化物对应的水化物不能反应生成盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com