
【化学——选修3:物质结构与性质】(15分)
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了 ,B元素位于周期表五个区域中的 区。

②ACl2分子中A的杂化类型为 ,ACl2的空间构型为 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
②六氰合亚铁离子[Fe(CN)6]4—中不存在 。
A.共价键
B.非极性键
C.配位键
D.σ键
E.π键
③写出一种与 CN—互为等电子体的单质分子式 。
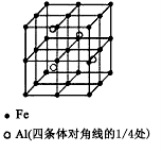
(3)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
①确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
(1) ①能量最低规则 (2分);s (2分)
②sp杂化 (1分);直线型 (1分)
(2) ①具有孤电子对(1分)
②B (2分)
③N2 (1分)
(3) ①Fe2Al (2分)
② (3分)
(3分)
【解析】
试题分析:(1)①根据能量最低原理,电子总是优先占据能量低的轨道,而该同学所画的电子排布图中3s轨道未排满就去排布3p轨道,所以违背了能量最低原理;根据B的电离能的数据可知,B元素是+2价金属,所以属于第二主族元素,位于元素周期表的s区,为Mg元素;
②根据表中数据可知A也是第二主族元素,因为A、B都是短周期元素,B是Mg,则A只能是Be元素,在BeCl2中,Be的价层电子对数是2+1/1(2-2)=2,所以Be原子是sp杂化;分子为直线型分子;
(2)①根据配合物的定义判断,一方提供空轨道,另一方提供孤电子对,Fe原子提供空轨道,所以与Fe原子或离子形成配合物的分子或离子应具备的结构特征是具有孤电子对;
②六氰合亚铁离子[Fe(CN)6]4—中,C与N原子之间是极性共价三键,所以存在σ键 和π键,CN与Fe原子之间是配位键,但不存在非极性键,所以答案选B;
③CN—中含有2个原子、10个价电子,所以与其互为等电子体的单质中含有2个原子、10个价电子,该分子式是N2;
(3)①根据均摊法,该晶胞中Fe原子的个数是8×1/8+6×1/2+12×1/4+1=8,Al原子全部位于体内,共4个Al原子,所以该晶胞中Fe与Al的原子个数比是2:1,其化学式是Fe2Al;
②此合金中最近的两个Fe原子之间的距离为晶胞棱长的一半,设晶胞的棱长为xcm,则4×139/NA/a3=ρ ,所以
a= ,则此合金中最近的两个Fe原子之间的距离为a/2=
,则此合金中最近的两个Fe原子之间的距离为a/2= 。
。
考点:考查物质的结构与性质的应用


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:选择题
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρg·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是
①
②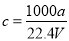
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④将50g上述溶液加入一定量的水稀释成0.5 c mol·L-1,则加入水的体积应大于50mL
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省新余市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.某溶液中由水电离出的c(OH-) = 1×10-amol·L-1,若a>7时,则该溶液的pH一定为14-a
B.等体积、等物质的量浓度的Na2SO3溶液与NaHSO3溶液混合:c(Na+) = c(SO32-) + c(HSO3-) + c(H2SO3)
C.将0.2mol·L-1的某一元酸HA溶液和0.1mol·L-1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH-)+c(A-)=2c(H+)+c(HA)
D.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(Na+)>2c(R2-)+c(HR-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通市高三第一次模拟化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.马口铁(镀锡铁皮)镀层破损后铁仍不易腐蚀
B.CH3Cl(g)+Cl2(g)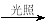 CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
C.MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)< Ksp(MnS)
D.合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通市高三第一次模拟化学试卷(解析版) 题型:选择题
下列各装置能够达到相应实验目的的是

A.用装置甲除去乙酸乙酯中混有的少量乙酸
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙制取无水MgCl2
D.用装置丁制取乙烯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省枣阳市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是

A.图I所示装置用于Cu和浓H2SO4制取少量的SO2气体
B.图Ⅱ装置可验证非金属性:Cl>C>Si
C.图Ⅲ可用于收集气体H2、CO2、Cl2、NH3
D.图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三第五次检测考试理综化学试卷(解析版) 题型:填空题
【化学——选修5:有机化学基础】(15分)
化合物H可用以下路线合成:
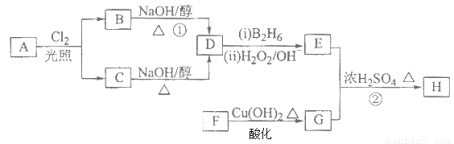
已知:
请回答下列问题:
(1)标准状况下11.2L烃A在氧气中充分燃烧可以生成88gCO2和45gH2O,且A分子结构中有3个甲基,则A的结构简式为 ;
(2)B和C均为一氯代烃,D的名称(系统命名)为 ;
(3)在催化剂存在下1molF与2molH2反应,生成3—苯基—1—丙醇。F的结构简式是 ;
(4)反应①的反应类型是 ;
(5)反应②的化学方程式为 ;
(6)写出所有与G具有相同官能团的芳香类同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市八校高三第二次联考化学试卷(解析版) 题型:填空题
(10分)A、B、C、D为原子序数依次增大的四种短周期元素,其性质或结构信息如下表:
元素 | A | B | C | D | E |
性质 或结 构信 息 | 室温下单质呈气态,原子最外层电子数与D相同 | D3B中阳离子与阴离子的电子层结构相同 | A和C可形成两种常见的化合物甲和乙,甲有强氧化性 | 单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体 | E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分 |
试回答以下问题
(1)B在周期表中的位置是 ,B的氢化物与E的氢化物比较,沸点较高的是 (填化学式)。
(2)D3B可与水反应生成2种碱性物质,请写出这一化学方程式 。
(3)写出丙的电子式为 。说明丙在空气中漂白的原理(用化学方程式表示) 。(请参考下表数据)
酸 | 电离常数 |
HClO | Ka=3.0×10-8 |
H2CO3 | Ka1=4.3×10-7,Ka2=5.6×10-11 |
(4)由B、C、D四种元素中的三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈碱性。将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成蓝色溶液,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省淮北市高三第一次模拟考试化学试卷(解析版) 题型:选择题
用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示。下列有关说法错误的是

A.H2A的物质的量浓度为0.1000mol.L-1
B.H2A是二元弱酸
C.a-b段发生反应HA-+OH-=H2O+A2-
D.a点时HA-的水解程度大于电解程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com