
下列各项操作中,“不发生先产生沉淀,然后沉淀又溶解”现象的是
①向饱和碳酸钠溶液中通入过量的CO2;②向NaAlO2溶液中逐滴加入过量的稀盐酸;③向AlCl3溶液中逐滴加入过量稀氢氧化钠溶液;④向硅酸钠溶液中逐滴加入过量的盐酸
A.①②  B.①③
B.①③
C.①④ D.②③
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
已知:2CrO42-(黄色)+2H+  Cr2O72-(橙色)+H2O。现以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下(阳离子交换膜只允许阳离子通过):
Cr2O72-(橙色)+H2O。现以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下(阳离子交换膜只允许阳离子通过):
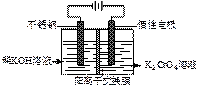
下列说法不正确的是
A.在阴极室,发生的电极反应为:2H2O+2e-=2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为产生的H+,与CrO42-离子反应使2CrO42-+2H+  Cr2O72-+H2O向右进行
Cr2O72-+H2O向右进行
C.该制备过程总反应的化学方程式为:
4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr )为d,则此时铬酸钾的转化率为1-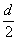
查看答案和解析>>
科目:高中化学 来源: 题型:
醋酸和氢氧化钠溶液发生反应的离子方程式正确的是
A.H++OH-→H2O B.H++ NaOH→Na++H2O
C.CH3COOH +OH-→CH3COO- +H2O D.CH3COOH + NaOH→CH3COO-+ Na++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应在生产、生活中具 有广泛的用途。下列做法中涉及到铝元素的还原性的是
有广泛的用途。下列做法中涉及到铝元素的还原性的是
A.明矾净化水
B.用氢氧化铝治疗胃酸过多
C.用铝制容器存放浓硫 酸
酸
D.电解熔融氧化铝制单质铝
查看答案和解析>>
科目:高中化学 来源: 题型:
以色列科学家谢赫特曼因发现铝合金中的原子是以准晶体排列且硬度很高,而荣获诺贝尔奖。下列关于铝及其化合物的说法正确的是
A.铝元素比硅元素在地壳中的含量高
B.所有的铝合金遇浓硫酸、浓硝酸均能钝化
C.等质量的铝与足量的盐酸、氢氧化钠反应放出的氢气质量相等
D.等物质的量的明矾与Ba(OH)2反应的离子方程式为:
Al3++2SO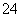 +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO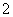 +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH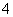 、Mg2+、Al3+、Fe3+、CO
、Mg2+、Al3+、Fe3+、CO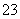 、SO
、SO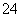 、NO
、NO 中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是

A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH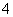 )=0.2 mol
)=0.2 mol
C.溶液中一定不含CO ,可能含有SO
,可能含有SO 和NO
和NO
D.n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加________,该过 程的现象为:_____________________________________________________________。
程的现象为:_____________________________________________________________。
(2)步骤②加入过量H2O2的目的是:______________________________________。
(3)步骤③中反应的离子方程式是:_______________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用,下列说法不正确的是
A.氧化镁用作耐火材料
B.Na2O常用于潜水艇或呼吸面具的供氧剂
C.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
D.FeCl3溶液可用于刻制印刷铜电路板
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com