
A.3X+YƒZ B.2X+YƒZ
C.X+3YƒZ D.3X+2Yƒ2Z
科目:高中化学 来源: 题型:


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:013
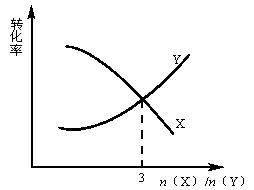
在一定条件下将X和Y两种气体按不同比例放入密闭容器中,反应达到平衡后,测得X和Y的转化率与起始时两物质的物质的量之比![]() 关系如图所示,则X和Y的化学方程式可表示为( )
关系如图所示,则X和Y的化学方程式可表示为( )
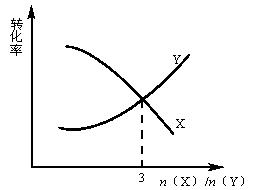
A.3X+YƒZ B.2X+YƒZ
C.X+3YƒZ D.3X+2Yƒ2Z
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北衡水中学高三上学期期中考试化学试卷(解析版) 题型:填空题
按要求填空
(一)、X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的一种单质具有特殊臭味,Z与X原子最处层电子数相同。回答下列问题:
(1)由上述元素组成的化合物中,既含有极性共价键又含有离子键的化合物的电子式 ;
(2)X和Y组成的化合物中,有一种既含有极性共价键又含有非极性共价键。此化合物可将碱性工业废水中的CNˉ氧化为碳酸盐和氨,相应的离子方程式为
(二)、在一定条件下,RO3nˉ 和Iˉ 发生反应,离子方程式为: RO3nˉ+6Iˉ+6H+==Rˉ+3I2+3H2O
RO3nˉ-中R元素的化合价为 ,R元素的原子最外层电子有 个。
(三)、Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1︰16,则x值是
(四)、已知M2On2ˉ可与R2ˉ作用,R2ˉ被氧化为R的单质,M2On2ˉ的还原产物中,M为+3价,又知c(M2On2ˉ)=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com