
| A. | 向碳酸氢钙溶液中加入少量烧碱溶液:Ca2++2HCO3-+20H-═CaCO3↓+CO32-+H2O | |
| B. | 碘水中通入足量的 S02:I2+SO2+2H2O═2I-+S042-+4H+ | |
| C. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O═A1O2-+4NH4++2H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(0H)3反应生成Na2FeO4:3ClO+2Fe(OH)3═2FeO32-+3Cl-+H2O+4H+ |
分析 A.氢氧化钠少量,所有的碳酸根离子都转化成碳酸钙沉淀;
B.碘单质能够将二氧化硫氧化成硫酸;
C.一水合氨为弱碱,二者反应生成氢氧化铝沉淀;
D.强碱性溶液中,反应产物中不会生成氢离子.
解答 解:A.向碳酸氢钙溶液中加入少量烧碱溶液,二者反应生成碳酸钙沉淀、碳酸氢钠和水,正确的离子方程式为:Ca2++HCO3-+OH-═CaCO3↓+H2O,故A错误;
B.碘水中通入足量的 SO2,二者发生氧化还原反应生成硫酸和HI,反应的离子方程式为:I2+SO2+2H2O═2I-+SO42-+4H+,故B正确;
C.向氯化铝溶液中滴加过量氨水,反应生成氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,正确的离子方程式为:4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:解答题
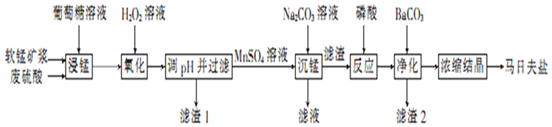
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.8 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
| Mn2+ | 7.8 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
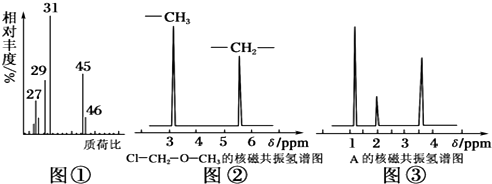
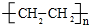 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
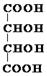 .
.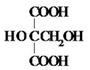 .M的核磁共振氢谱图中有4组吸收峰.
.M的核磁共振氢谱图中有4组吸收峰.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
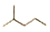 ,其分子式为C6H14,名称是2-甲基戊烷,它可由2种炔通过加成反应得到.
,其分子式为C6H14,名称是2-甲基戊烷,它可由2种炔通过加成反应得到.| 实验步骤 | 解 释 或 实 验 结 论 |
| (1)称取A 18.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①A的相对分子质量为90. |
(2)A的核磁共振氢谱如图: | ②A中含有4种氢原子. |
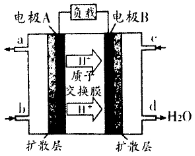
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大量塑料废弃物会造成严重的白色污染,应将其焚烧处理 | |
| B. | 应用放射性同位素发射出的射线,可进行食物保鲜和肿瘤治疗 | |
| C. | 过度开采使用煤、石油等化石燃料,会导致空气中PM2.5浓度升高 | |
| D. | 近两年全国普遍取消了各种节日焰火晚会,对减缓空气污染起到了一定作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
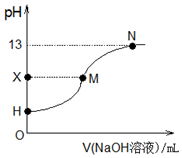
| A. | 酸碱滴定选用指示剂:甲基橙试液 | |
| B. | H点处的溶液:pH<3 | |
| C. | X=7时,M点对应加入氢氧化钠溶液的体积:25.00 mL | |
| D. | H、M、N三点各自对应的溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
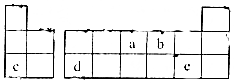
| A. | 气态氢化物的稳定性:a>b>c | |
| B. | 原子半径大小:a>b>c | |
| C. | c,d,e的氧化物对应的水化物之间两两皆能反应 | |
| D. | b、c形成的化合物中阴、阳离子的个数比为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com