
| A. | 离子化合物中一定含有金属阳离子和阴离子 | |
| B. | 离子键是阴、阳离子通过静电作用形成的,NaCl熔化时破坏了离子键 | |
| C. | N2分子中含有的共价键很强,故N2分子比较稳定 | |
| D. | 共价键既可存在于共价化合物中,也可存在于离子化合物或非金属单质中 |
分析 A、氯化铵是离子化合物,但不含金属离子;
B.阴、阳离子以离子键结合;
C.结构决定性质,氮气分子中氮氮之间是叁键,键能大,分子稳定;
D.多原子单质、离子化合物和共价化合物中可能含有共价键.
解答 解:A、氯化铵是离子化合物,但不含金属离子,所以离子化合物中不一定含金属阳离子,故A错误;
B.阴、阳离子以离子键结合,即离子键是阴、阳离子通过静电作用形成的化学键,所以NaCl熔化时破坏了离子键,故B正确;
C.结构决定性质,氮气分子中氮氮之间是叁键,键能大,分子稳定,故C正确;
D.多原子单质、离子化合物和共价化合物中可能含有共价键,如氮气分子中存在氮氮共价键、离子化合物氯化铵中含氮氢共价键,故D正确;
故选A.
点评 本题考查了物质与化学键的关系,难度不大,注意:离子化合物中可能存在共价键,为易错点.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题


 .
. (苯环上有两个取代基,其中有一个甲基在对位且属于酯类).
(苯环上有两个取代基,其中有一个甲基在对位且属于酯类).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 装置 | 分别进行的实验 | 现象 |
 | i.连好装置 一段时间后,向烧杯中滴加酚酞 | 碳棒附近溶液变红 |
| ii.连好装置 一段时间后,向烧杯中滴加[K3[Fe(CN)6] | 铁片表面产生蓝色沉淀 |
| 实验 | 滴加 | 试管 | 现象 |
 | 0.5mol.LK3[Fe(CN)6]溶液 | iii.蒸馏水 | 无明显变化 |
| iv.1.0mol•L-1NaCl溶液 | 铁片表面产生大量蓝色沉淀 | ||
| v.0.5mol•L-1Na2SO4溶液 | 无明显变化 |
| 实验 | 试剂 | 现象 |
| A | 酸洗后的铁片K3[Fe(CN)6]溶液(已除O2) | 产生蓝色沉淀 |
| B | 酸洗后的铁片K3[Fe(CN)6]和NaCl混合溶液(未除O2) | 产生蓝色沉淀 |
| C | 铁片K3[Fe(CN)6]和NaCl混合溶液(已除O2) | 产生蓝色沉淀 |
| D | 铁片K3[Fe(CN)6]和盐酸混合溶液(已除O2) | 产生蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | A是原电池,B是电解池 | |
| B. | 同温同压下,a电极消耗气体和d电极产生气体体积相等 | |
| C. | 当电路中通过2mole-,A、B中各有2molH+通过隔膜,但移动方向相反 | |
| D. | c电极的电极反应方程式为:N2O4+2HNO3-2e-═2N2O5+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 含氯苯(
含氯苯( )的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其除去原理如图所示,下列叙述正确的是( )
)的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其除去原理如图所示,下列叙述正确的是( )| A. | A极为负极,发生氧化反应 | B. | H+由A极穿过质子交换膜到达B极 | ||
| C. | A 极电极反应式为 +2e-+H+=Cl-+ +2e-+H+=Cl-+ | D. | 反应后电解液的pH升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
| B | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中一定有SO42- |
| C | 向10mL 0.2mol/LNaOH溶液中先滴入2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液 | 先有白色沉淀生成,加入FeCl3溶液后,又有红褐色沉淀生成 | 在相同的温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中一定无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
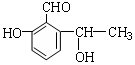 某有机物的结构简式如图,它可能发生的反应类型有( )
某有机物的结构简式如图,它可能发生的反应类型有( )| A. | ①②③④⑥ | B. | ②③④⑤⑧ | C. | ③④⑤⑥⑦ | D. | ①②③⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com