
【题目】下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
C.漂白粉、活性炭、![]() 都能使红墨水褪色
都能使红墨水褪色
D.![]() 和
和![]() 溶液使酸性高锰酸钾的紫色褪去
溶液使酸性高锰酸钾的紫色褪去
科目:高中化学 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如下:

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_________________________;
(2)“溶解”时放出的气体为_______________ (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为______________________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式_____________;

(5)金属铬在溶液中有多种存在形式, CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应________________,根据A点数据计算出该转化反应的平衡常数为______________,温度升高,溶液中CrO42—的平衡转化率减小,则该反应的△H____0(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(加试题)紫杉醇![]() 是一种抗癌药,化合物D是紫杉醇的侧链,D的合成路线如下
是一种抗癌药,化合物D是紫杉醇的侧链,D的合成路线如下![]() 图示中结构
图示中结构![]() 为苯基
为苯基![]() :
:
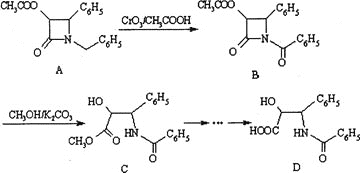
![]() 下列说法不正确的是________。
下列说法不正确的是________。
A.有机物A的分子式是![]()
B.有机物A和B结构中具有相同的官能团
C.有机物D能发生的有机反应类型有酯化、水解、加成、消去和缩聚反应
D.上述四种有机物在酸性条件下均能发生水解反应,且都能得到同一种水解产物
![]() 的合成应用了2010年诺贝尔化学奖的获奖成果
的合成应用了2010年诺贝尔化学奖的获奖成果![]() 交叉偶联反应,反应式如下
交叉偶联反应,反应式如下![]() 已配平
已配平![]() :
:![]()
![]()
![]()
X分子中含碳氮双键![]() ,其结构简式为________。
,其结构简式为________。
![]() 已知酯和酰胺在过量醇中能发生醇解反应:
已知酯和酰胺在过量醇中能发生醇解反应:
CH3COOC2H5+CH3OH![]() CH3COOCH3+C2H5OH
CH3COOCH3+C2H5OH
![]() +CH3OH
+CH3OH![]()
![]() +CH3COOCH3
+CH3COOCH3
写出B转化为C的化学方程式是________。
![]() 若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F。写出同时符合下列条件的E的所有同分异构体的结构简式________。
若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F。写出同时符合下列条件的E的所有同分异构体的结构简式________。
①结构中含有![]()
②遇氯化铁溶液发生显色反应
③1H-NMR谱显示分子中有四种不同化学环境的氢原子
![]() 已知:
已知:
①RCHO![]()
![]()
②R’COOH![]() R’COCl
R’COCl
采用甲醛和乙醛为原料制备![]() ,请设计合成路线_____________。
,请设计合成路线_____________。![]() 无机试剂任选
无机试剂任选![]() 。合成路线流程图示例如下:
。合成路线流程图示例如下:
CH3CH2OH![]() H2C=CH2
H2C=CH2![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、C1-)生产CuCl的流程:
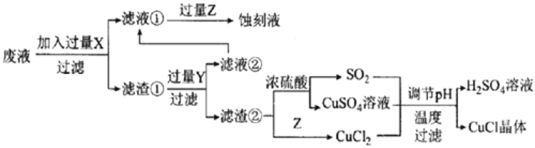
已知:CuCl是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,在空气中迅速被氧化为绿色,见光分解变成褐色。
请回答下列问题:
(1)流程中的滤渣①与Y反应和X与Y反应相比,单位时间内得到的气体多,其原因为____________________________________________。
(2)滤液①需要加过量Z,检验Z过量的方法是______________________。
(3)写出生成CuCl的离子方程式:_________________________________。
(4)为了提高CuCl产品的纯度,流程中的“过滤”操作适宜用下列装置图中的___________(填选项字母),过滤后,洗涤CuCl的试剂宜选用___________(填“无水乙醇”或“稀硫酸”)

(5)CuCl加入饱和NaCl溶液中会部分溶解生成CuCl2-,在一定温度下建立两个平衡:
I. CuCl (s) ![]() Cu +(aq)+Cl- (aq) Ksp=1.4×10-6
Cu +(aq)+Cl- (aq) Ksp=1.4×10-6
II. CuCl(s)+Cl- (aq)![]() CuCl2-(aq) K=0.35。
CuCl2-(aq) K=0.35。
分析c(Cu+)、c(CuCl2-)和Ksp、K的数学关系,在图中画出c(Cu+)、c(CuCl2-)的关系曲线(要求至少标出一个坐标点) ______。

(6)氯化亚铜的定量
①称取样品0.25g于250mL锥形瓶中,加入10mL过量的FeCl3溶液,不断摇动:
②待样品溶解后,加入20mL蒸馏水和2滴指示剂;
③立即用0.1000mol·L-1硫酸铈标准溶液滴定至绿色为终点;
④重复三次,消耗硫酸铈溶液的平均体积为24.30mL。
上述相应化学反应为CuCl+ FeCl3===CuCl2+FeCl2、Fe2++Ce4+===Fe3++Ce3+,则样品中CuCl的纯度为___________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(9分)某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是 ,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)
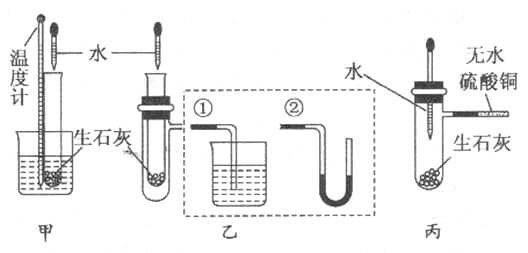
乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①) ,(接②) ,说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是 ,说明反应放热,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将正确答案的序号填在空白处。
(1)用经![]() 消毒的自来水配制下列溶液:①
消毒的自来水配制下列溶液:①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() ;⑤
;⑤![]() ;⑥稀盐酸,发现部分药品变质,它们是 ______ 。
;⑥稀盐酸,发现部分药品变质,它们是 ______ 。
(2)下列反应必须加入氧化剂且一步反应就能完成的是 ______ 。
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
(3)在如图所示的8个装置中,属于原电池的是 ______ 。
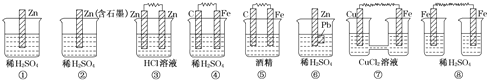
(4) ①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。
①②相连时,外电路电流从②流向①;
②③相连时,③为正极;
②④相连时,②上有气泡逸出;
③④相连时,③的质量减少.
据此判断这四种金属活动性由大到小的顺序是 ______ 。
(5)下列物质中,不能由单质直接化合生成的是 ______ 。
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
(6)下列物质中,属于强电解质的是 ______ ;属于非电解质的是 ______ 。
①氨气②氨水③盐酸④醋酸⑤硫酸钡⑥氯化银 ⑦氯化钠⑧二氧化碳⑨醋酸铵⑩氢气![]() 水
水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:X2(g)+3Y2(g) ![]() 2Z2(g),若X2、Y2、Z2的初始物质的量浓度分别为0.10mol·L-1、0.30mol·L-1、0.20mol·L-1,当反应达到平衡时Z2的物质的量浓度不可能是
2Z2(g),若X2、Y2、Z2的初始物质的量浓度分别为0.10mol·L-1、0.30mol·L-1、0.20mol·L-1,当反应达到平衡时Z2的物质的量浓度不可能是
A. 0.05mol·L-1 B. 0.20mol·L-1 C. 0.35mol·L-1 D. 0.40mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ![]() 。
。
A.![]() 溶于足量稀
溶于足量稀![]() :
:![]()
B.用食醋检验牙膏中碳酸钙的存在:![]()
C.![]() 酸性溶液放在空气中变质:
酸性溶液放在空气中变质:![]()
D.电解![]() 水溶液的离子方程式: 2Cl-+2H2O
水溶液的离子方程式: 2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com