
| A. | ①②⑤ | B. | ②③④ | C. | ①③⑤ | D. | ①③④ |
科目:高中化学 来源: 题型:选择题
| A. | 原子半径Y>Z>X>W | B. | 氢化物的稳定性H2Y>HZ | ||
| C. | 离子的氧化性aW3+>bX+ | D. | a+3<c-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ②④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥⑦ | B. | ③⑤⑦ | C. | ③⑥⑦ | D. | ②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
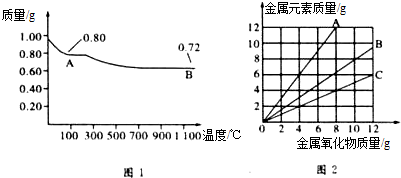
| A. | 图1中,A到B的过程中有0.005mol电子发生了转移 | |
| B. | 图1整个过程中共生成0.18g水 | |
| C. | 图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A | |
| D. | 图1中A和B化学式分别为Cu2O和CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 测定等物质的量浓度的盐酸、硅酸的pH | 盐酸的pH小于硅酸的pH | 非金属性:Cl>Si |
| B | 取待测液于试管中,加一颗绿豆大的钠粒 | 有气体生成 | 检验乙酸溶液中是否混有乙醇 |
| C | 向FeI2溶液中加入少量苯,然后再通入少量Cl2 | 下层液体呈浅绿色,上层液体呈紫红色 | 还原性:I->Fe2+ |
| D | 加热分解某盐X,将产生的气体通入硝酸酸化的BaCl2溶液中 | 产生白色沉淀 | X可能是NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com