
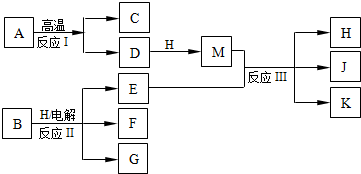
���� A��BΪ�����C����������֮һΪCO2��D��K���������������Ϸ�Ӧ�����ж�ΪDΪCaO��AΪCaCO3��H������ΪҺ̬�������ƶ�ΪH2O��MΪCa��OH��2��J��һ�־���Ư�����õ����ƶ�ΪCa��ClO��2��KΪCaCl2��EΪCl2����ӦIII��E��G��Ӧ��ԭ����ͬ��˵��GΪ���Ϸ�Ӧ�����������ƶ�BΪNaCl�������Һ��Ӧ���ɲ���GΪNaOH��FΪH2�������ƶϳ������ʽ��з����ش��������⣮
��� �⣺��ӦI����ӦII�ͷ�ӦIII���ǹ�ҵ�����г����ķ�Ӧ��A��BΪ�����C����������֮һΪCO2��D��K���������������Ϸ�Ӧ�����ж�ΪDΪCaO��AΪCaCO3��H������ΪҺ̬�������ƶ�ΪH2O��MΪCa��OH��2��J��һ�־���Ư�����õ����ƶ�ΪCa��ClO��2��KΪCaCl2��EΪCl2����ӦIII��E��G��Ӧ��ԭ����ͬ��˵��GΪ���Ϸ�Ӧ�����������ƶ�BΪNaCl�������Һ��Ӧ���ɲ���GΪNaOH��FΪH2��
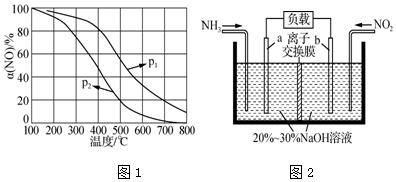
��1����Ӧ���ǵ缫����ʳ��ˮ�ķ�Ӧ����Ӧ�����ӷ���ʽΪ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
��2��J��Ca��ClO��2�����ú��㲻�Ӵ�ˮ������������Ҳ�ֽ�����K��CaCl2�������ų������������÷�Ӧ�Ļ�ѧ����ʽ��Ca��ClO��2=CaCl2+O2����
�ʴ�Ϊ��Ca��ClO��2=CaCl2+O2����
��3���ٵⵥ����������Һ��������Na2S2O3����Һ�ζ�I2ʱѡ�õ�ָʾ��Ϊ���ۣ�����Na2S2O3����Һ�ĵ��룬��ɫ��ȥ��
�ʴ�Ϊ�����ۣ�
������I2�ķ�Ӧ�����ӷ���ʽΪ��ClO-+2I-+2H+=Cl-+I2+H2O��
�ʴ�Ϊ��ClO-+2I-+2H+=Cl-+I2+H2O��
��4������0.1mol E��Cl2��ͨ��100mL FeBr2��Һ�У���Һ��������֮һ��Br-��������Br2����Һ��Fe2+�Ļ�ԭ�Դ���Br-�Ļ�ԭ�ԣ�ͨ��������������Fe2+���ӣ���Ӧ��ȫ��������Br-��
��FeBr2��Һ��ҺŨ��Ϊx����Fe2+���ʵ���Ϊ0.1xmol����Br-���ʵ���Ϊ0.2mol��Cl2���ʵ���Ϊ0.1mol��������Һ��������֮һ��Br-��������Br2�õ���
Cl2+2Br-=Br2+2Cl-��
1 2
$\frac{0.1x}{3}$ $\frac{1}{3}$��0.2x
�����������ӷ�Ӧ���������ʵ���=0.1mol-$\frac{0.1x}{3}$
Cl2 +2Fe2+=2Fe3++2Cl-��
1 2
0.1mol-$\frac{0.1x}{3}$ 0.1x
��ʽ����õ�x=1.2mol/L��
�ʴ�Ϊ��1.2��
���� ���⿼���˹�ҵ�����г����ķ�ӦӦ�ã�����ʽ��д�����ӷ���ʽ����д���������ʵ�Ӧ�ã���Ӧ���������Ͳ������ʷ����ж��ǽ���ؼ���


 ���ĺ����Ͼ�������ϵ�д�
���ĺ����Ͼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ���� | C�� | ��֬ | D�� | ��ά�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������մɡ����� | B�� | ������մɡ����Ժ���ĥ�� | ||
| C�� | ���ᱵ�մɡ������� | D�� | �������մɡ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ޢۢڢܢ٢� | B�� | �ݢܢۢ٢ڢ� | C�� | �ޢۢ٢ڢܢ� | D�� | �ڢۢ٢ܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������������Һ��ϳ�����ʱ����Һ�д��ڣ�c��Na+��=c��HC2O4-��+c��C2O42-�� | |
| B�� | NaHC2O4��NaClO��Һ��ϣ���Ӧ�����ӷ���ʽΪ��HC2O4-+ClO-=HClO+C2O42- | |
| C�� | �������Һ�У�c��NH4+��=2 c��H2C2O4��+2 c��HC2O4-��+2 c��C2O42-�� | |
| D�� | ����ʹ����KMnO4��Һ��ɫ�������ӷ���ʽΪ��5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
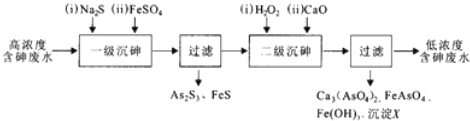
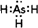
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2��O3��Ϊͬ�������� | B�� | 16O��18O��������Ų���ͬ | ||
| C�� | ��ѿ�������ǻ�Ϊͬ���칹�� | D�� | CH3CH3��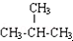 ��Ϊͬϵ�� ��Ϊͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com