
| A. | 正极反应为:14H2O+7O2+28e-=28OH- | |
| B. | 放电过程中KOH的物质的量浓度减小 | |
| C. | 每消耗1molC2H6,则电路上转移的电子为14mol | |
| D. | 放电一段时间后,负极周围的pH升高 |
分析 在燃料电池中,负极上是燃料发生失电子的氧化反应,C2H6+18OH--14e-═2CO32-+12H2O,正极上是氧气发生得电子的还原反应,2H2O+O2+4e-═4OH-,根据电极反应可以确定电子转移情况以及电极附近溶液的酸碱性变化情况.
解答 解:A、在燃料电池中,正极上是氧气发生得电子的还原反应,14H2O+7O2+28e-=28OH-,故A正确;
B、根据总反应为:2C2H6+7O2+8KOH═4K2CO3+10H2O,可以知道放电过程中,消耗了氢氧化钾,KOH的物质的量浓度会减小,故B正确;
C、根据负极电极反应式:C2H6+18OH--14e-═2CO32-+12H2O,每消耗1molC2H6,则电路上转移的电子数为14mol,故C正确;
D、根据负极反应:C2H6+18OH--14e-═2CO32-+12H2O,放电一段时间后,该极上消耗氢氧根离子,所以负极周围的pH降低,故D错误;
故选D.
点评 本题考查学生燃料电池的工作原理知识,注意书写电极反应时结合溶液的酸碱性分析,难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | pH=3的某酸跟pH=11的某碱等体积混合,往其中滴加酚酞,溶液变红 | 生成强碱弱酸盐 |
| B | Mg(OH)2(s)加入CH3COONH4溶液中,固体溶解 | NH4+与OH-结合成NH3•H2O 使Mg(OH)2的溶解平衡右移 |
| C | 室温下,用pH试纸测得:0.lmol•Na2SO3溶液的pH约为10;0.lmol•L-1NaHSO3溶液的pH约为 5 | HSO3-结合H+的能力SO32-的弱 |
| D | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用过程中,电极正极E溶液的pH增大 | |
| B. | 使用过程中,溶液中氢氧根向Ag2O电极移动 | |
| C. | 使用过程中.电子由Ag2O极经外路流向Zn极 | |
| D. | 使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 0.05mol | C. | 1.05mol | D. | 0.11mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水煤气是二次能源 | B. | 水力是二次能源 | ||
| C. | 石油是二次能源 | D. | 电能是一次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
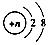 ,下列有关该粒子的说法中不正确的是( )
,下列有关该粒子的说法中不正确的是( )| A. | M粒子的符号可能是O2-、Ne、Mg2+等 | |
| B. | n值只有5种可能 | |
| C. | 取含有M粒子的溶液进行焰色反应,若为黄色,则M的符号是Na+ | |
| D. | n=13时,含M粒子的溶液加入过量的氨水,最终有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是直线形结构 | |
| B. | 中心原子都采取 sp1杂化 | |
| C. | 硫原子和碳原子上都没有孤对电子 | |
| D. | SO2 为 V 形结构,CO2为直线形结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com