
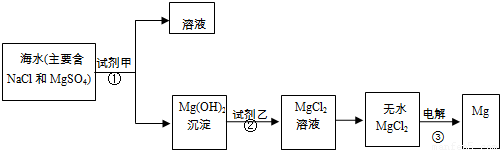
 Mg+Cl2↑,元素的化合价发生了变化,是氧化还原反应;
Mg+Cl2↑,元素的化合价发生了变化,是氧化还原反应;

科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
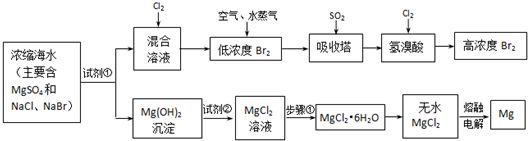
| ||
| ||
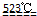 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑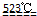 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑查看答案和解析>>
科目:高中化学 来源: 题型:

| 方法 | 是否正确 | 简述理由 |
| 方法1:直接往海水中加入沉淀剂 | 不正确 | (一) |
| 方法2:高温加热蒸发海水后,再加入沉淀剂 | (二) | (三) |
| 你认为最合理的其他方法是:(四) | ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| 是否正确 | 简述理由 | |
| 学生1的观点 | 否 否 |
海水中镁离子浓度小,沉淀剂的用量大,不利于镁离子的沉淀 海水中镁离子浓度小,沉淀剂的用量大,不利于镁离子的沉淀 |
| 学生2的观点 | 否 否 |
能源消耗大,海水的综合利用低,成本高 能源消耗大,海水的综合利用低,成本高 |
| 学生3的观点 | 是 是 |
镁离子富集浓度高,成本低 镁离子富集浓度高,成本低 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
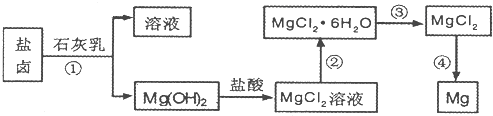
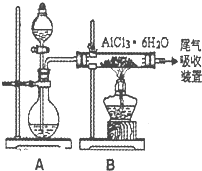
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com