
 ,B的结构简式
,B的结构简式 或
或 ;
;分析 A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,则原子个数之比为1:1,符合CnH2n-6,B的相对分子质量为78,则12n+2n-6=78,解得n=6,所以B为苯,以此来解答.
解答 解:A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,则原子个数之比为1:1,符合CnH2n-6,B的相对分子质量为78,则12n+2n-6=78,解得n=6,所以B为苯,以此来解答.
(1)由以上分析可知A为乙烯,电子式为 ,B为苯,结构简式为:
,B为苯,结构简式为: 或
或  ,
,
故答案为: ;
; 或
或  ;
;
(2)A相邻的同系物C为CH2=CHCH3,使溴水褪色发生加成反应,该反应为:CH2=CHCH3+Br2→CH2BrCHBrCH3,
故答案为:CH2=CHCH3+Br2→CH2BrCHBrCH3;
(3)碘水中加入苯发生萃取,苯的密度比水的小,则苯在上层,观察到下层无色,上层紫红色,
故答案为:溶液分层,下层无色,上层紫红色;
(4)设A、B的质量都为m,由CxHy消耗x+$\frac{y}{4}$氧气,可知等质量的A、B完全燃烧时消耗O2的物质的量分别为$\frac{3m}{28}$mol和$\frac{15m}{156}$mol,所以等质量的A、B完全燃烧时消耗O2的物质的量A>B,
故答案为:A>B.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,明确A为乙烯B为苯,并熟悉乙烯与苯的化学性质即可解答,注意等质量的乙烯与苯中H的质量分数越大消耗氧气越大,题目难度不大.


科目:高中化学 来源: 题型:解答题
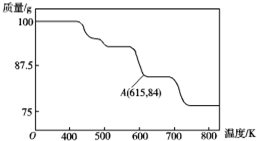 铬(Cr)有许多种化合物,在工业生产中有广泛的用途.
铬(Cr)有许多种化合物,在工业生产中有广泛的用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除④⑦外 | B. | 除③⑥外 | C. | ①②⑤ | D. | 除④外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应物 | 催化剂 | 温度 | |
| A | 10mL20% H2O2溶液 | 无 | 40℃ |
| B | 10mL20% H2O2溶液 | 无 | 25℃ |
| C | 10mL20% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 | 40℃ |
| D | 10mL10% H2O2溶液 | 无 | 25℃ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热金属铝使之熔化 | B. | 液态SO3受热蒸发 | ||
| C. | 加热HI气体使之分解 | D. | 加热石英晶体使之熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
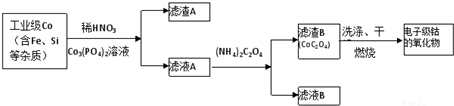
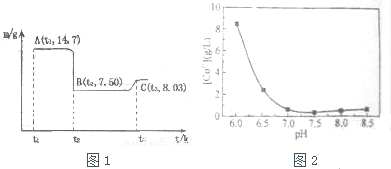
| 开始沉淀的pH | 完全溶解的pH | |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Co2+ | 7.2 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
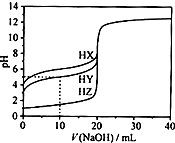 25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )| A. | 在相同温度下,同浓度的三种酸溶液的酸性强弱顺序:HZ<HY<HX | |
| B. | HZ、HY、HX均为弱酸 | |
| C. | 向HY溶液中加入10.00mLNaOH溶液,一定有c(Y-)+c(OH-)═c(H+)+c(Na+) | |
| D. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com