
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( ) 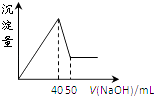
A.1:3
B.1:2
C.1:1
D.2:1
【答案】C
【解析】解:首先发生反应Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,然后发生反应Al(OH)3+OH﹣═AlO2﹣+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为10mL,根据离子方程式Al3++3OH﹣═Al(OH)3↓可知,生成Al(OH)3沉淀消耗的氢氧化钠溶液的体积=3×10mL=30mL,图象显示,生成沉淀总共消耗氢氧化钠溶液40mL,则生成氢氧化镁沉淀需要氢氧化钠的体积为10mL,
根据Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓知,镁离子和铝离子的物质的量之比为1:2,根据原子守恒知,Al2(SO4)3与MgSO4的物质的量浓度之比= ![]() =1:1,故选C.
=1:1,故选C.
首先发生反应Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,然后发生反应Al(OH)3+OH﹣═AlO2﹣+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为10mL,根据离子方程式Al3++3OH﹣═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的体积,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液40mL,计算沉淀Mg2+消耗的氢氧化钠溶液的体积,从而确定溶液中n(Mg2+):n(Al3+),再根据原子守恒确定其浓度之比.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】NH3在工业生产上有重要的应用
(1)写出用浓氨水检验氯气管道泄漏的化学反应方程式
(2)若将少量氨气与过量氯气混合,则生成一种酸和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C都是金属:B中混有C时,只有C能被盐酸溶解;A与B与稀硫酸组成原电池时,A为电池的正极。A、B、C三种金属的活动性顺序为( )
A. A>B>CB. A>C>BC. C>B>AD. B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读、分析下列两个材料:
材料一、如图
材料二
物质 | 熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 溶解性 |
乙二醇( C2H6O2) | ﹣11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题:
(1)要从氯化钠和纯碱的固体混合物中分离得到纯净的氯化钠,应先将固体溶解,再经过、洗涤、干燥等操作.
(2)将乙二醇和丙三醇相互分离的最佳方法是 , 写出该方法在操作上的注意事项(写出一项) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有A+ , B3+ , C3+ 三种金属阳离子的水溶液发生了如下一系列变化后逐一沉淀出来,其中B3+转入白色沉淀: 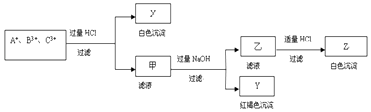
请通过分析回答(用化学符号填写):
(1)A+是 , B3+是 , C3+是;
(2)X是 , Y是 , Z是;
(3)写出下列离子方程式:
①生成Y沉淀:;②B3+与过量氨水反应:;
(4)写出下列化学方程式:单质铝和Y分解后的固体产物反应: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示的装置蒸馏海水,下列说法正确的是( )
A.实验时冷却水应从a进入,从b流出
B.蒸馏烧瓶中要加入碎瓷片,目的是防止暴沸
C.锥形瓶中能收集到高浓度的氯化钠溶液
D.该装置可用于分离海水中的NaCl和MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】橡胶属于重要的工业原料,它是一种有机高分子化合物,具有良好的弹性,但强度较差。为了增加某些橡胶制品的强度,加工时往往需要进行硫化处理(即橡胶原料与硫磺在一定条件下反应)。橡胶制品的硫化程度越高,强度越大,弹性越差。下列橡胶制品中,加工时硫化程度较高的是
A. 橡皮筋 B. 汽车外胎
C. 普通气球 D. 医用乳胶手套
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com