
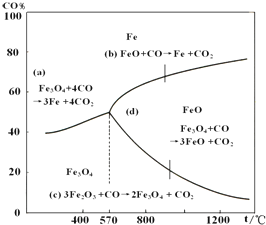
 ������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯���������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ��������CO����������Ĺ�ϵ��ͼ��
������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯���������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ��������CO����������Ĺ�ϵ��ͼ��| 1 |
| 6 |
| 1 |
| 6 |
| 1 |
| 6 |
| 4.48L |
| 22.4L/mol |
| x |
| 0.2-x |
| 2 |
| 35 |
| 2 |
| 35 |
| ||
| 7.2g |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ksp��AgI��С��Ksp��AgCl��g��AgI����ת��ΪAgCl | ||||
| B�������������Ksp���Խ���������Խ����ת��Ϊ�����ܵ������� | ||||
| C��AgI��AgCl��������ˮ������AgCl����ת��ΪAgI | ||||
D�������£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻����
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ba2++SO42-�TBaSO4�� |
| B��Fe+2H+�TFe2++H2�� |
| C��Al2O3+6H+�T2Al3++3H2O |
| D��HCO3-+OH-�TCO32-+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
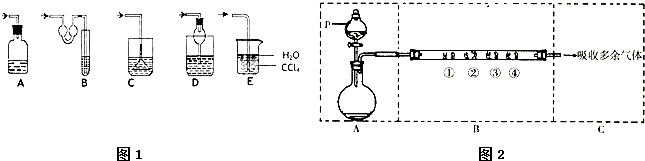
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� |
B�� |
C�� |
D��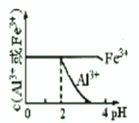 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | �����Ϣ |
| X | X�ǵؿ��к�������Ԫ�� |
| Y | YԪ��ԭ�Ӻ���3p�ܼ�����4������ |
| Z | ����Z��������Ϊ14��������Ϊ7 |
| T | T�ĵ�����һ�ֳ����Ľ����������Ƶ�������������Һ�����ڼ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
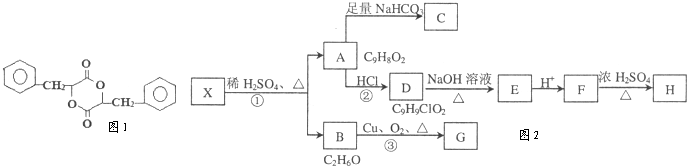
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���¶�һ��ʱ������Һ��c��Ag+����c��Cl-��=Kspʱ������ҺΪAgCl�ı�����Һ |
| B��AgNO3��Һ��NaCl��Һ��Ϻ����Һ�У�һ����c��Ag+��=c��Cl-�� |
| C����AgClˮ��Һ�м������ᣬKspֵ��� |
| D��������AgCl���뵽��Ũ��KI��Һ�У�����AgClת��ΪAgI��AgCl�ܽ��С��AgI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
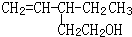 ����һ���Ĺ�ѧ���ԣ������о�����ʹ������ʧȥ��ѧ���Եķ���
����һ���Ĺ�ѧ���ԣ������о�����ʹ������ʧȥ��ѧ���Եķ����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com