
| A. | 0.32mol/(L•s) | B. | 0.16mol/(L•s) | C. | 0.8mol/(L•s) | D. | 0.08mol/(L•s) |
分析 先计算氨气浓度变化量,然后根据物质的变化浓度之比等于化学计量数之比求出氮气的浓度变化量,最后根据v=$\frac{△c}{△t}$计算反应的速率.
解答 解:起始时氨气的物质的量为4mol,5s时为2.4mol,氨气浓度变化量为(4mol-2.4mol)÷2L=0.8mol/L,物质的变化浓度之比等于化学计量数之比,所氮气的浓度变化为0.4mol/L,则用氮气表示该反应的速率v=$\frac{△c}{△t}$=$\frac{0.4mol/L}{5s}$=0.08mol/(L•s),故选D.
点评 本题考查化学反应速率有关计算,比较基础,常用方法有定义法与化学计量数比值法,根据情况选择合适的计方法.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(ClO)2溶液中通入少量SO2:Ca2++3ClO-+SO2+H2O═CaSO3↓+Cl-+2HClO | |
| B. | 1 mol/L的NaAlO2溶液和2.5 mol/L的盐酸等体积均匀混合:2AlO2-+5H+═Al(OH)3↓+Al3++H2O | |
| C. | 将11.2L标准状况下的氯气通入200mL2mol/L的FeBr2溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2═2Fe3++4Br2+10Cl- | |
| D. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+═Fe2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
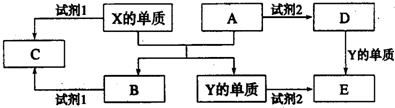
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氯气及其相关产品在生活、生产中应用广泛.
氯气及其相关产品在生活、生产中应用广泛.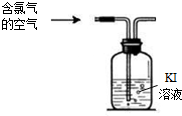
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该硫酸的物质的量浓度为1.84mol/L | |
| B. | 若 Zn与该硫酸反应消耗13克Zn,一定产生4.48升气体 | |
| C. | 配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL | |
| D. | 该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 任何条件下,等物质的量的Cl2和HCl所含的分子数必相等 | |
| C. | 1LHCl气体一定比1L Cl2气体的质量小 | |
| D. | 22.4LHCl气体的物质的量恰好是11.2LHCl气体的物质的量的二倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素是具有相同核电荷数的同一类原子的总称 | |
| B. | 核素代表一类原子 | |
| C. | 某元素的一种核素代表该元素的一种原子 | |
| D. | 某种同位素或核素代表该元素的一种原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
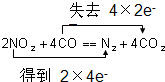
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com