
【题目】下列实验操作和结论错误的是( )
A.用新制![]() 悬浊液可鉴别麦芽糖和蔗糖
悬浊液可鉴别麦芽糖和蔗糖
B.用银镜反应可证明淀粉是否水解为葡萄糖,但不能证明其是否完全水解
C.浓硫酸可使蔗糖变黑,证明浓硫酸具有脱水性
D.向蔗糖溶液中滴加几滴稀硫酸后,水浴加热几分钟,将混合液再加入到银氨溶液中,不能发生银镜反应,则证明蔗糖没有发生水解
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.NH3中氮原子的杂化方式为sp3杂化
B.[Cu(NH3)4]2+中,NH3是配体
C.NH4+、PH4+、CH4、BH4-互为等电子体
D.NH3的沸点比PH3的沸点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物的应用广泛。试回答下列问题:
(1)基态![]() 原子的价电子轨道表示式为__________,其第一电离能比
原子的价电子轨道表示式为__________,其第一电离能比![]() 的__________(填“大”或“小”)。
的__________(填“大”或“小”)。
(2)氨硼烷(![]() )被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的原子是__________,写出一种与氨硼烷互为等电子体的有机小分子:___________________(填化学式)。
)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的原子是__________,写出一种与氨硼烷互为等电子体的有机小分子:___________________(填化学式)。
(3)常温常压下硼酸(![]() )的晶体结构为层状,其二维平面结构如图所示。
)的晶体结构为层状,其二维平面结构如图所示。
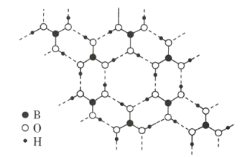
①B原子的杂化方式为__________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大: _________________。
②路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯分子中不存在碳碳单键和碳碳双键的交替结构,下列可以证明该结论的事实是( )
①苯不能使酸性![]() 溶液褪色 ②苯分子中碳碳键的键长完全相等 ③苯能在加热和催化剂存在的条件下与氢气发生反应生成环己烷 ④经实验测得对二甲苯只有一种结构 ⑤苯在溴化铁作催化剂条件下与液溴可发生取代反应,但不能因发生化学反应而使溴水褪色
溶液褪色 ②苯分子中碳碳键的键长完全相等 ③苯能在加热和催化剂存在的条件下与氢气发生反应生成环己烷 ④经实验测得对二甲苯只有一种结构 ⑤苯在溴化铁作催化剂条件下与液溴可发生取代反应,但不能因发生化学反应而使溴水褪色
A.②③④B.②④⑥C.①②⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学研究小组制备硝基苯的实验装置如图所示,相关数据见下表。已知该实验中存在的主要副反应是:在温度稍高的情况下会生成间二硝基苯。
物质 | 熔点/℃ | 沸点/℃ | 密度/( | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
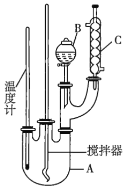
实验步骤如下:
取![]() 浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心加入
浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心加入![]() 中。取
中。取![]() 苯加入
苯加入![]() 中。在室温下,向苯中逐滴加入混合酸,边滴加边搅拌,混合均匀加热,使其在/span>50~60℃下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、
中。在室温下,向苯中逐滴加入混合酸,边滴加边搅拌,混合均匀加热,使其在/span>50~60℃下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、![]() 溶液和水洗涤。在分出的产物中加入无水
溶液和水洗涤。在分出的产物中加入无水![]() 颗粒,静置片刻,过滤,对滤液进行蒸馏纯化,收集205~210℃的馏分,得到纯硝基苯
颗粒,静置片刻,过滤,对滤液进行蒸馏纯化,收集205~210℃的馏分,得到纯硝基苯![]() 。
。
回答下列问题:
(1)图中装置![]() 的作用是______。
的作用是______。
(2)制备硝基苯的化学反应方程式为___________。
(3)配制混合酸时,能否将浓硝酸加入到浓硫酸中?_____(填“能”或“不能”),说明理由:_______。
(4)为了使反应在50-60 ℃下进行,常采用的加热方法是_____。反应结束并冷却至室温后![]() 中液体为粗硝基苯,粗硝基苯呈黄色的原因是_________。
中液体为粗硝基苯,粗硝基苯呈黄色的原因是_________。
(5)在洗涤操作中,第二次水洗的目的是____。
(6)本实验所得到的硝基苯的产率是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用乙醇制备溴乙烷:CH3CH2OH+HBr![]() CH3CH2Br+H2O,但通常采用溴化钠和浓硫酸与乙醇共热的方法。下面是某同学对该实验的猜想,你认为可能错误的是( )
CH3CH2Br+H2O,但通常采用溴化钠和浓硫酸与乙醇共热的方法。下面是某同学对该实验的猜想,你认为可能错误的是( )
A.制备过程中可能看到有气泡产生
B.可以将适量的NaBr、H2SO4(浓![]() 、CH3CH2OH三种药品置入一种容器中加热制备CH3CH2Br
、CH3CH2OH三种药品置入一种容器中加热制备CH3CH2Br
C.如在夏天做制备CH3CH2Br的实验,实际收集到的产物可能较少
D.为了除去CH3CH2Br中混有的HBr,可用热的NaOH溶液洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)是第三代半导体材料,具有热导率高、化学稳定性好等性质,在光电领域和高频微波器件应用等方面有广阔的前景。
(1)传统的氮化镓制各方法是采用GaC13与NH3在一定条件下反应。NH3的电子式为___。
(2)Johnson等人首次在1100℃下用液态镓与氨气制得氮化镓固体,该可逆反应每生成1 mol H2放出10.3 kJ热量。其热化学方程式为_________。
(3)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示。
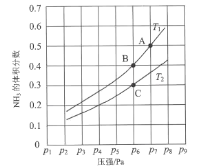
①下列说法正确的是___(填标号)。
a. 温度:T1>T2
b. 当百分含量ω(NH3)=ω(H2)时,说明该反应处于化学平衡状态
c. A点的反应速率小于C点的反应速率
d. 温度恒定为T2,达平衡后再充入氦气(氦气不参与反应),NH3的转化率不变
②既能提高反应速率又能使平衡正向移动的措施有___(写出一条即可)。
③气体分压(p分)=气体总压(p总)×体积分数,用平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp)。在T2时,用含p6的计算式表示C点的______。
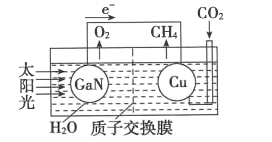
(4)如图可表示氮化镓与铜组装成的人工光合系统的工作原理。H+向______(填“左”或“右”)池移动;铜电极上发生反应的电极反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氨基酸中含C、N、H、O四种元素,已知除氢原子外,其他原子均达到最外层8电子的稳定结构。如图为该氨基酸分子的球棍模型:
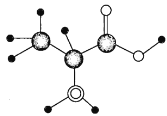
(1)氨基酸是_________(填“淀粉”“纤维素”“蛋白质”或“油脂”)完全水解的产物,该氨基酸的结构简式为__________。
(2)该氨基酸中含氧官能团的名称是____________。
(3)在浓硫酸、加热的条件下,该氨基酸与乙醇发生酯化反应的化学方程式为______。
(4)互为同系物的有机物具有相同的官能团,与该氨基酸互为同系物且少一个碳原子的氨基酸的结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某线型高分子化合物的结构简式如图所示:
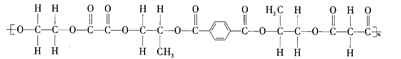
下列有关说法正确的是( )
A.该高分子化合物是由4种单体缩聚而成的
B.形成该高分子化合物的几种羧酸单体互为同系物
C.形成该高分子化合物的单体中的乙二醇可被![]() 催化氧化生成草酸
催化氧化生成草酸
D.该高分子化合物有固定的熔沸点,1mol该高分子化合物完全水解需要氢氧化钠的物质的量为5nmol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com