
| A. | 升温、水溶液中盐类水解平衡、弱酸的电离平衡、沉淀溶解平衡不一定朝正向移动 | |
| B. | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝变红色;反复数次,试管中的液体出现刺激性气味,标明乙醇已被铜氧化为乙醛 | |
| C. | 我国古化文献《本草经集注》记载区分硝石(KNO3)与朴硝(Na2SO4):“以火烧之,紫青烟起,乃真硝石也”,是应用了焰色反应知识 | |
| D. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 |
分析 A.盐类水解、弱酸电离为吸热反应,而沉淀溶解平衡有的吸热、有的放热;
B.由现象可知,Cu与氧气反应生成CuO,CuO氧化乙醇生成乙醛、Cu、水;
C.硝石(KNO3)与朴硝(Na2SO4)灼烧时呈现K、Na的焰色反应;
D.催化剂具有选择性,会影响目标产物在最终产物中的比例.
解答 解:A.盐类水解、弱酸电离为吸热反应,而沉淀溶解平衡有的吸热、有的放热,则升高温度沉淀溶解平衡不一定朝正向移动,故A正确;
B.由现象可知,Cu与氧气反应生成CuO,CuO氧化乙醇生成乙醛、Cu、水,则Cu不能氧化乙醇,Cu在该反应中作催化剂,故B错误;
C.硝石(KNO3)与朴硝(Na2SO4)灼烧时呈现K、Na的焰色反应,则应用了焰色反应知识,故C正确;
D.催化剂只能对主反应即生成目标产物的那个反应起起作用,这样在转化率一定的时候的确目标产物的比例会加大,故D正确;
故选B.
点评 本题考查较综合,涉及物质的性质、应用及盐类水解、焰色反应等,为高频考点,把握物质的性质、发生的饭为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化、液化均为化学变化,而石油的常压蒸馏和减压蒸馏均是物理变化 | |
| B. | 绿色化学的核心就是利用化学原理吸收处理工业生产污染物并将其转化为有用物质 | |
| C. | 利用石油的裂化可以提高汽油的产量和质量 | |
| D. | 将苦卤水浓缩、氧化,鼓入空气和水蒸气可提取溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H6 | C. | C2H5OH | D. | CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
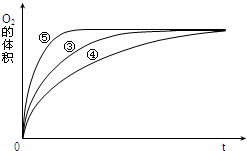 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 浓 时间 度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将苯和溴水混合后加入Fe粉制溴苯 | |
| B. | 为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,振荡,若无油滴浮在液面上,说明油脂已完全反应 | |
| C. | 检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热煮沸,观察是否出现红色沉淀 | |
| D. | 探究化学反应的限度:取5ml 0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5-6滴,充分反应,根据溶液中是否含有碘单质和碘离子判断该反应有一定限度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com