
(15分)某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验室按以下步骤进行:
①称量a g样品,置于烧杯中;
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全;
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤、洗涤沉淀;
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量;
请根据上面叙述,回答:
(1)下图所示仪器中,本实验步骤①②③中必须用到的仪器是E和 (填字母)。
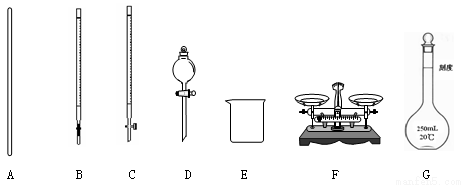
(2)写出步骤③中发生反应的离子方程式 。
(3)洗涤是洗去附着在沉淀上的 (写离子符号),洗涤沉淀的操作是 。
(4)如何确定沉淀是否洗涤干净的操作是 。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为 。(列出算式,不需化简)
(6)该兴趣小组中甲学生认为:实验步骤③中不加入氯水,其余步骤不变,仍可达到实验目的。你认为甲学生的观点是否正确? (填正确或错误);请说明理由: 。
(共15分)
(1)(2分)A C F G
(2)(2分)2Fe2++Cl2=2Fe3++2Cl-
(3)(4分)NH4+、Cl-、OH-;向漏斗里注入蒸馏水,使水面没过滤渣,等水自然流完后,重复操作2~3次。
(4)(2分)取最次一次洗出液,滴加AgNO3溶液若无沉淀产生,则证明已洗净。
(5)(2分)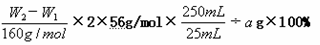
(6)(3分)正确;氯化铁溶液中Fe3+水解Fe3++3H2O?Fe(OH)3+3H+,加热HCl挥发,促进水解进行,过一系列转化最终都能生成Fe2O3对后续实验无影响。
【解析】
试题分析:(1)称量时需要天平、钥匙;溶解时需要烧杯、玻璃棒;配制一定物质的量浓度的溶液时需要量筒、烧杯、玻璃棒、胶头滴管、一定规格的容量瓶;准确量取溶液需要酸式滴定管、洗耳球,故答案为:A C F G。
(2)氯水能将FeCl2氧化生成FeCl3,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-。
(3)溶液中含有氨水、氯化铵,所以离子有:NH4+、Cl-、OH-;洗涤沉淀的方法是向漏斗里注入蒸馏水,使水面没过滤渣,等水自然流完后,重复操作2~3次。
(4)加入过量的氨水,氢氧化铁生成表面附着有氯化铵、氨水等,故附着的离子有NH4+、Cl-、OH-等,所以确定沉淀是否洗涤干净的操作是:取最次一次洗出液,滴加AgNO3溶液若无沉淀产生,则证明已洗净。
(5)铁元素质量守恒,即红棕色固体中的铁就是样品中铁,Fe2O3中铁元素的质量为(W2-W1)g×112/160,样品中铁元素的质量(W2-W1)g×112/160×250/25,样品中铁元素的质量分数为: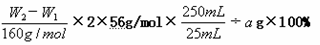
(6)氯化铁溶液中Fe3+水解Fe3++3H2O?Fe(OH)3+3H+,加热HCl挥发,促进水解进行,过一系列转化最终都能生成Fe2O3对后续实验无影响。
考点:本题考查溶液的配制、实验方案的分析与评价、物质含量的测定、化学计算。


科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
(12分)Ⅰ、现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=________;
(2)丙溶液中存在电离平衡为______________________(用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为_________;
Ⅱ、某一元弱酸(用HA表示)在水中的电离方程式是HA ??H++A-,回答下列问题:
??H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向________(填“正”、“逆”)反应方向移动,理由是_______________________________________。
(2)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”、“碱”或“中”)。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:实验题
(13分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量,请填写下列空白:
移取10.00 ml密度为ρ g/mL的过氧化氢溶液至烧杯后全部将其转移到250 ml (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
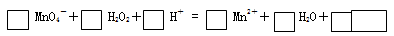
(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4)复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)请将他们的实验方法和实验现象填入下表:
实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
验证氧化性 |
|
|
验证不稳定性 |
|
|
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是( )
⑴Cl2+2KI=2KCl+I2; ⑵2FeCl2+Cl2=2FeCl3;
⑶2FeCl3+2HI=2FeCl2+2HCl+I2,⑷H2S+I2=S+2HI;
A.S>I2>Fe3+>Cl2 B.Cl2>Fe3+>I2>S
C.Fe3+>Cl2>S>I2 D.Cl2>I2>Fe3+>S
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
市场上销售的“84”消毒液,其商品标识上有如下叙述:①本品为无色液体,呈碱性②使用时加水稀释③可对餐具、衣物进行消毒,可漂白浅色衣物。其有效成分可能是( )
A.Cl2 B.SO2 C.NaClO D.KMn04
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
现将1mo1Cu2S与144克FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2 、CuSO4的混合溶液,并产生NO气体。则最终消耗的硝酸的物质的量是
A.12mo1 B.15mo1 C.16mo1 D.17mo1
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42- 等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,

下列说法正确的是
A.d点溶液中含有的溶质有Na2SO4 、NaAlO2、NH3?H2O
B.原溶液中含有的Fe3+、Mg2+和Al3+的物质的量之比为1:1:1
C.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓, Mg2++2OH—= Mg(OH)2↓,Fe3++3OH-=Fe(OH)3↓
D.原溶液中含有的阳离子必定有H+、NH4+、Al3+,但不能肯定Mg2+和Fe3+中的哪一种
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪第一中学高三9月摸底考试化学试卷(解析版) 题型:填空题
(12分)如下表所示为自然界中的多种铜矿石的主要成分:
矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3·Cu(OH)2 |
请回答:
(1)上表所列铜化合物中,铜的质量百分含量最高的是 (填化学式);
(2)工业上以黄铜矿为原料。采用火法溶炼工艺生产铜。该工艺的中间过程包含反应:
2Cu2O+Cu2S 6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是 ;
6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是 ;
(3)火法溶炼工艺生产铜的尾气直接排放到大气中造成环境污染的后果是 ;处理该尾气可得到有价值的化学品,写出其中一种酸和一种盐的名称或化学式 、 。
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母)。
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 铜绿的主成分是碱式碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
C | 铁比铜活泼 | 铆在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中质量检测化学试卷(解析版) 题型:选择题
下列类型的反应,一定发生电子转移的是
A.化合反应 B.置换反应 C.复分解反应 D.分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com