
【题目】科学家预言自然界中可能存在原子序数为114号的稳定同位素![]() X,根据原子结构理论和元素周期律下列预测错误的是
X,根据原子结构理论和元素周期律下列预测错误的是
A.![]() X位于第七周期,第ⅣA 族B.X是金属元素
X位于第七周期,第ⅣA 族B.X是金属元素
C.XO2是酸性氧化物D.X元素的化合价有+2和+4
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】以石墨为电极分别电解水和饱和食盐水,关于两个电解池反应的说法正确的是( )
A.阳极反应式相同
B.电解结束后所得液体的pH相同
C.阴极反应式相同
D.通过相同电量时生成的气体总体积相等(同温同压)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氟酸为弱酸。25℃时将0.1mol·L-1的HF加水不断稀释,下列表示的量保持不变的是( )
①n(H+);②c(H+)·c(OH—);③c(OH—)+c(F—);④![]() ;⑤
;⑤![]() ;
;
A.①③④B.②③④C.③④⑤D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,将H2和I2各1 mol的气态混合物充入1 L的密闭容器中,发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH<0; 5 min后达到平衡状态,测得c(H2)=0.9 mol·L-1,则下列结论中,不能成立的是
2HI(g) ΔH<0; 5 min后达到平衡状态,测得c(H2)=0.9 mol·L-1,则下列结论中,不能成立的是
A. 平衡时H2、I2的转化率相等
B. 若将容器温度提高,其平衡常数K一定增大
C. 其他条件不变再向容器中充入少量H2,I2的转化率提高
D. 从反应开始至平衡的过程中,v(HI)=0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴是一种重的化工原料,从淡化海水中提取溴的工艺流程如下:
![]()
⑴操作Ⅱ中,用饱和Na2CO3碱性溶液吸收Br2,过程中有CO2产生,反应的粒子方程式为______,当0.6 mol Br2被吸收时,转移电子的数目为______
![]() 步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有______
步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有______![]() 填序号
填序号![]()
a.烧杯 b.分液漏斗c.普通漏斗 d.玻璃棒 e.蒸发皿 f.冷凝管
![]() 某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
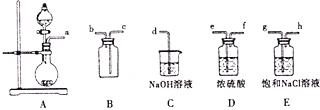
①将A,B,C相连,制得Cl2后加入适量水,即可制得氯水,将所得氯水分为两份,进行甲,乙两个实验,实验操作如下,将现象填入下表:
实验序号 | 实验操作 | 现象 |
甲 | 将氯水滴入品红溶液 | ______ |
乙 | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |
②由实验乙不能推出氯气与水反应的产物具有酸性,原因是______,若要制备纯净干燥的Cl2,按气流方向连接各仪器接口,顺序为a→_____→_____→_____→_____→_____→_____→d
![]() 实验完毕后,假设装置C中氢氧化钠和
实验完毕后,假设装置C中氢氧化钠和![]() 恰好完全反应,其反应方程式为______,反应后溶液中离子浓度由大到小的顺序为______,常温下HClO的电离平衡常数为K,则常温下NaClO水解反应的平衡常数为______(用含Ka和Kw的表达式表示)
恰好完全反应,其反应方程式为______,反应后溶液中离子浓度由大到小的顺序为______,常温下HClO的电离平衡常数为K,则常温下NaClO水解反应的平衡常数为______(用含Ka和Kw的表达式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过下列装置可探究Cu2S(黑色)与O2的反应产物。下列说法错误的是
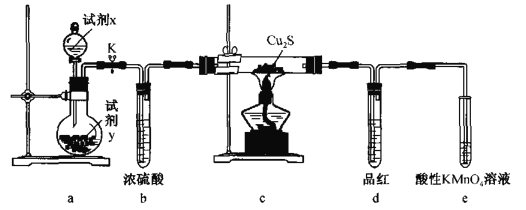
A.试剂x、y可分别选用H2O、Na2O2B.b、d的作用分别是干燥O2、检验SO2
C.若c中固体变红色,说明生成物为金属铜D.e中酸性KMnO4溶液可用NaOH溶液替代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O。将12g该有机物的完全燃烧产物通过浓硫酸,浓硫酸增重14.4g,再通过碱石灰,碱石灰增重26.4g。则该有机物的分子式为( )
A.C4H10B.C2H6OC.C3H8OD.C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列是有关R、W、X、Y、Z五种元素的叙述,其中正确的是
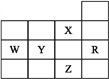
A. X元素是电负性最大的元素
B. p能级未成对电子最多的是Z元素
C. Y、Z的阴离子电子层结构都与R原子的相同
D. W元素的第一电离能小于Y元素的第一电离能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这三种离子的物质的量随消耗氯气物质的量的变化如下图所示。下列说法中正确的是( )
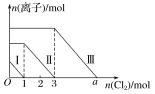
A.线段Ⅲ代表Fe2+的变化情况
B.线段Ⅰ代表Br-的变化情况
C.a值等于6
D.原混合溶液中n(FeBr2)=4mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com